
实验操作:将粗苯胺加入仪器B中,向仪器A中加水,打开F,加热仪器A使水沸腾。同时对仪器B进行预热,关闭F,让水蒸气导入蒸馏装置,通入冷凝水,开始蒸馏。
回答下列问题:
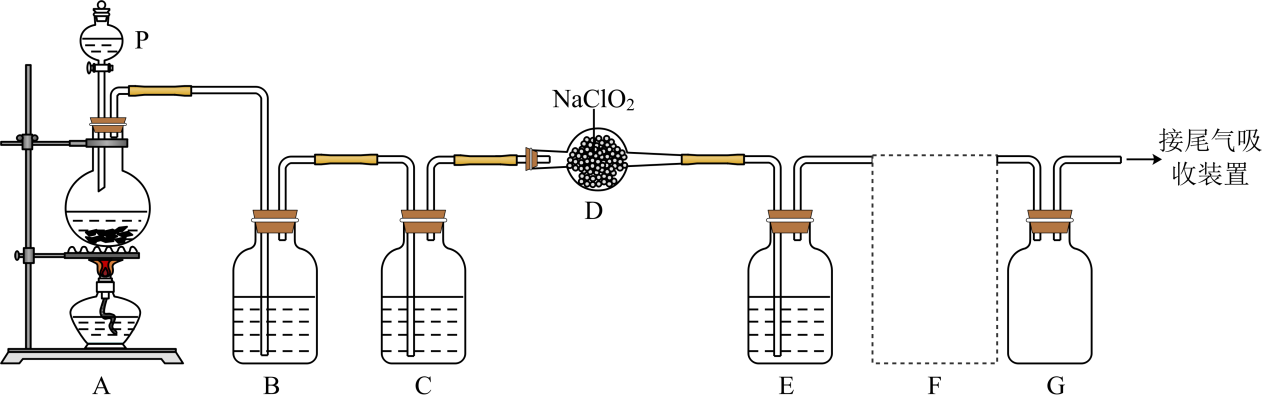
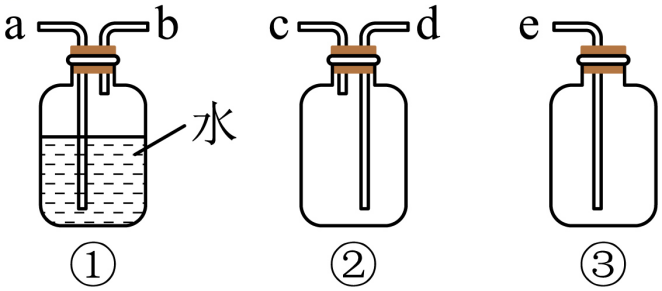
①请写出该反应的化学方程式:,每消耗319.5gNaClO3 , 生成L氯气(标况下)。(M(NaClO3)=106.5)。
②浓盐酸在该反应中表现出来的性质是(填序号)。
A. 只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性

简要步骤如下:
步骤Ⅰ:利用上图装置获取纯净;
步骤Ⅱ:取一只洁净而干燥的锥形瓶(E),用合适的橡胶塞塞紧后在塞子上作上标记,用电子天平称量,质量:.用E收集
.
集满后,在电子天平上称量,质量(+瓶+塞子):
.
步骤Ⅲ:分子量的测定
依据阿伏加德罗定律的推论: ,
可得:
请回答下列问题:
a.水 b.浓硫酸 c.无水氯化钙及玻璃纤维
d.饱和碳酸氢钠溶液 e.碱石灰及玻璃纤维

下列说法不正确的是( )

已知:
Ⅰ.光气与水易反应,能溶于溶液;
Ⅱ.有关物质熔沸点如下表。
物质 | ||||
熔点/℃ | 1435 | 1152 | -23 | -118 |
沸点/℃ | 4000 | 1300 | 76 | 8.2 |
①写出加入过量后反应的离子方程式。
②产品中质量分数为,若沉淀完全转变为
溶液后,不继续加热一段时间会导致质量分数(填“偏高”“偏低”或“不变”)。