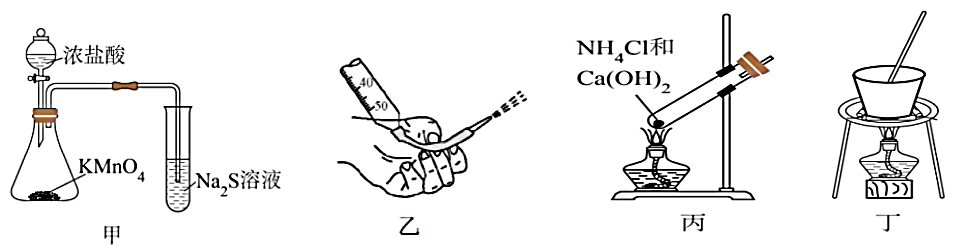
Ⅰ.往圆底烧瓶中加入2.5mL甲苯和140mL水,加热至沸,从仪器A上口(如图)分批加入10.4g 固体,最后用少量水将粘在仪器A内壁的
固体冲洗入圆底烧瓶内。
Ⅱ.继续煮沸并间歇性摇动圆底烧瓶,直至甲苯完全反应。
(反应方程式: )
)
Ⅲ.趁热过滤反应混合物,用少量热水洗涤滤渣,合并滤液和洗涤液,将滤液放在冷水浴中冷却,用浓硫酸酸化,使溶液从强碱性至强酸性,苯甲酸全部析出为止。
Ⅳ.过滤可得粗产品约2g。用重结晶法提纯。
Ⅴ.用碱滴定法测纯度,取0.1000g样品,溶于乙醇中,加入10mL水和2滴酚酞,用0.02mol/L NaOH溶液滴定。
回答下列问题。
a.加入约100mL水(75℃)配制成热的浓溶液;
b.加半匙活性炭;
c.用少量沸水淋洗烧杯和漏斗中的固体,合并滤液;
d.搅拌下将溶液煮沸3~5min,趁热过滤;
e.冷却结晶,过滤、洗涤、晾干得苯甲酸纯品。
序号 | 1 | 2 | 3 | 4 |
样品质量/g | 0.1000 | 0.1000 | 0.1000 | 0.1000 |
耗酸体积/mL | 8.00 | 8.02 | 7.98 | 8.96 |


已知:
回答下列问题:
准确称取样品,用容量瓶配成
溶液;取
上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置
;用
标准溶液滴定至溶液呈微黄色,加入淀粉指示剂继续滴定至终点,消耗
溶液
。
①该样品的有效氯测定值为%。
该样品的有效氯=×100%)
②下列操作会导致样品的有效氯测定值偏高的是(填字母)。
A.滴定管在滴定前仰视,滴定后俯视
B.盛装标准溶液的滴定管未润洗
C.滴定管在滴定前无气泡,滴定后有气泡
D.碘量瓶中加过量的稀硫酸