
①盐酸的浓度 ②镁条的表面积 ③溶液的温度 ④Cl-的浓度
①
②
,
。
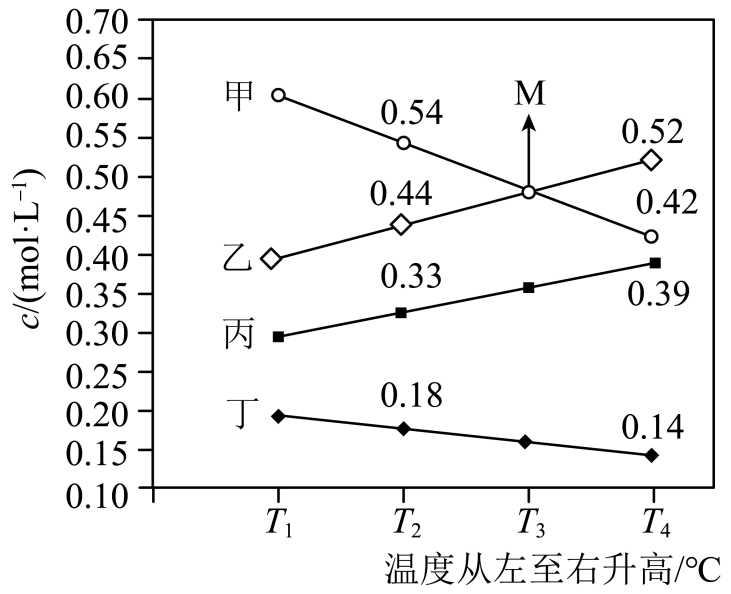
①甲是(填化学式),写出该反应的化学方程式:。
②正反应(填“>”“<”或“=”)0,判断依据是
③T3℃时NH3的平衡转化率为。

①CO的平衡转化率a=;T1℃时,反应平衡常数k=(保留2位有效数字)。
②由T1℃时上述实验数据计算得到v正~x(CO)和v逆~x(H2)的关系如图1所示。若升高温度,反应重新达到平衡,则v正~x(CO)相应的点变为、v逆~x(H2)相应的点变为。


间接制取低碳烯烃:CO(g)+2H2(g)CH3OH(l) △H1=-116kJ•mol-1
2CH3OH(l) C2H4(g)+2H2O(l) △H2=-35kJ•mol-1
直接制取低碳烯烃:2CO(g)+4H2(g) C2H4(g)+2H2O(g) △H3
回答下列问题:



已知:该反应![]() 焓变和熵变受温度影响很小,可视为常数。200℃时,该反应____自发进行。
焓变和熵变受温度影响很小,可视为常数。200℃时,该反应____自发进行。

①420℃时NO转化率低于390℃时NO转化率的原因可能是。
②B点(填“是”或“否”)达到化学平衡状态,理由是。
状态 | 热值(kJ/g) | 沸点(℃) | 密度(kg/L) | 液态能量密度(MJ/L) | |
氨气 | 气 | 18.6 | -33 | 0.6820 | 12.7 |
氢气 | 气 | 120 | -253 | 0.0708 | 8.5 |
氮元素燃烧后生成的稳定产物为N2。请书写NH3燃烧的热化学方程式。