
操作 | 现象 | 结论或离子方程式 |
步骤1:取少量滤液a进行①(填实验名称)。 | 火焰呈②。 | 滤液a中含有 |
步骤2:另取少量滤液a于试管中,依次滴入③(填化学式)溶液和氯水。 | 溶液先无红色,后变红色。 | 滤液a中含有 |


I.样品分解:称取a g毒重石矿粉于烧杯中,加入稍过量的溶液,90℃下加热搅拌2h,待充分反应后,冷却,过滤。
II.除:向滤液中加入一定量的BaS溶液,有黑色沉淀生成,过滤。
III.结晶:将步骤II的滤液经过①,②,抽滤,用冷水和乙醇各洗涤晶体2~3次,自然晾干。
回答下列问题:

某学生查阅资料: , X代表
,
、
等,
代表
的阴离子,设计如下纯度测量方案:
步骤I.准确称取粗品并用20.0mL水溶解。
步骤II.用的
标准溶液滴定其中的
步骤III.重复滴定2~3次,记录每次消耗标准溶液的体积
①滴定时采用下图所示的侧边自动定零位滴定管,结合该装置的使用说明书分析其优点。

②下列选项所涉及内容会导致含量的测定值偏高的是(填序号)。
a.未干燥锥形瓶 b.标准溶液久置部分失效
c.滴定终点时滴定管尖嘴中产生气泡 d.杂质可与反应

①
②
③
下列说法正确的是____。
①分子中含有联苯结构(![]() )和
)和基团
②核磁共振氢谱中只有4组峰

①含有苯环,且有两个取代基;
②含有碳碳三键;
③既能发生水解反应又能发生银镜反应。
其中,核磁共振氢谱显示为四组峰,且峰面积比为3∶2∶2∶1的同分异构体的结构简式为。
 为原料,设计合成
为原料,设计合成 的路线:(无机试剂任选)。
的路线:(无机试剂任选)。
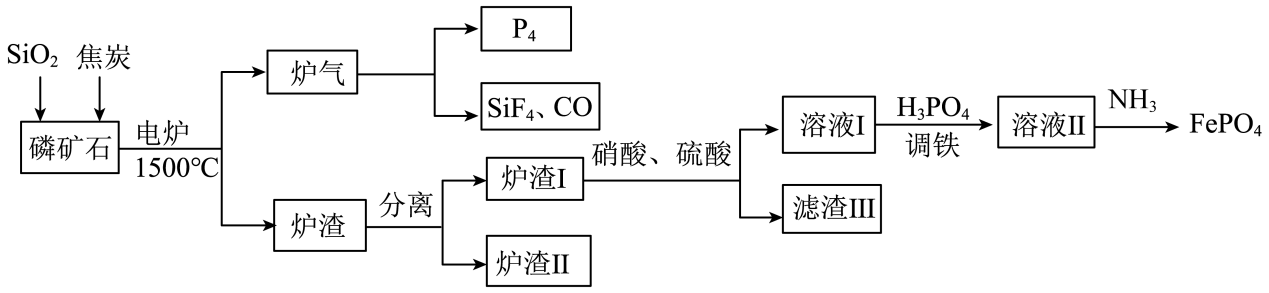
已知:①FePO4可溶于pH<2的酸性溶液。
②Fe3+在pH为2.0时开始沉淀,pH为4.0时沉淀完全。
回答下列问题:
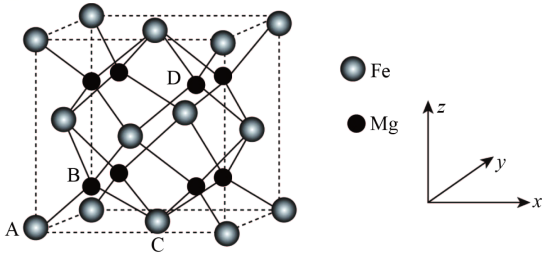
其中A的原子坐标参数为(0,0,0), B为( ,
,
),C为(
,
, 0),则D点的坐标参数为。此晶胞中Fe的配位数是。