 )是重要的化工原料,可由异丁醇(
)是重要的化工原料,可由异丁醇( )脱水制得。异丁醇催化脱水时发生如下反应:
)脱水制得。异丁醇催化脱水时发生如下反应:反应1(主反应):![]()
 (异丁烯,g)
(异丁烯,g)
反应2(副反应):2

保持压强为100MPa不变,向一定体积的密闭容器中充入V(异丁醇)的混合气体(
不参与反应),平衡时所得异丁醇的转化率、异丁烯的产率与温度的关系如图所示。下列说法错误的是( )

①
②
,
。
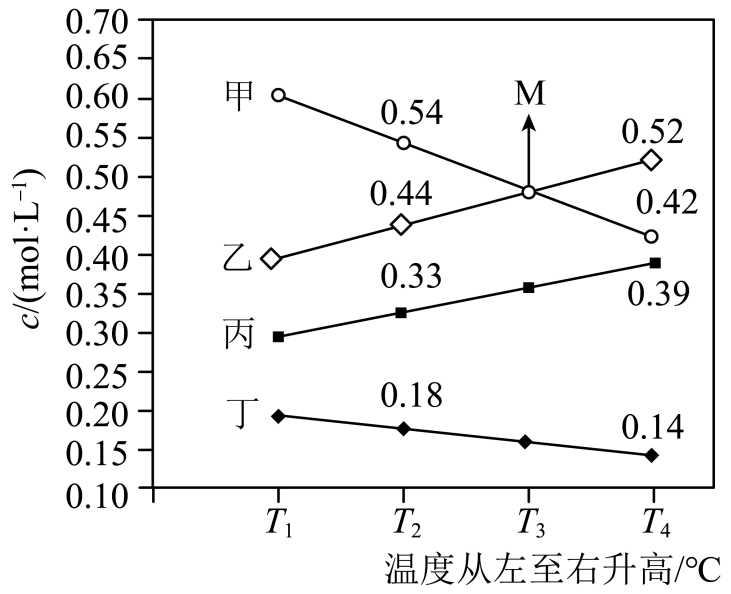
①甲是(填化学式),写出该反应的化学方程式:。
②正反应(填“>”“<”或“=”)0,判断依据是
③T3℃时NH3的平衡转化率为。
化学键 | C=O | H—O | H—H | C—O | C—H | C—C |
键能( | 803 | 463 | 436 | 326 | 414 | 348 |
依据表中数据计算的
H=
, 下列有利于该反应自发进行的条件是(填标号)。
A.高温 B.低温 C.任何温度

该反应中形成的化学键有____(填标号)。
a. b.容器中气体的平均摩尔质量不变
c.CH3CH2OH的百分含量保持不变 d.容器中混合气体的密度保持不变

①表示的曲线为(填标号)。
②、
、
由大到小的顺序是。
③℃、投料比为
下,该反应的平衡常数
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
温度/℃ | 220 | 240 | 250 | 255 |
BL/% | 60.2 | 84.6 | 92.6 | 95.2 |
| 1.2 | 1.8 | 1.9 | 2.1 |
| 0.2 | 0.3 | 0.4 | 0.6 |
已知:![]()
下列说法不正确的是( )
在下列温度下,该反应可能自发进行的是____(填字母)。

产物从催化剂上脱附(填“释放”或“吸收”)能量;该反应历程中有个基元反应,决速步骤的反应可以表示为。

在催化剂Ⅱ作用下的转化率随温度升高先增大后减小的原因可能是(不考虑温度对催化剂活性的影响);c点
(填“大于”或“小于”)b点
, 简述其原因:。
序号 | 反应速率 | |||
I | 0.1 | 0.1 | 0.1 | v |
II | 0.2 | 0.1 | 0.1 | |
III | 0.2 | 0.4 | 0.1 | |
IV | 0.1 | 0.9 | 0.3 |
则。


①CO的平衡转化率a=;T1℃时,反应平衡常数k=(保留2位有效数字)。
②由T1℃时上述实验数据计算得到v正~x(CO)和v逆~x(H2)的关系如图1所示。若升高温度,反应重新达到平衡,则v正~x(CO)相应的点变为、v逆~x(H2)相应的点变为。



使用催化剂的曲线是(填“甲”或“乙”),该催化剂可使反应历程中决速步骤的活化能降低eV,平衡转化率(填“增大”“减小”或“不变”)。达到化学平衡后再升高温度,正反应速率(填“加快”或“减慢”),平衡(填“正向”“逆向”或“不”)移动。

已知:选择性是指生成目标产物所消耗的反应物的物质的量与参与反应的反应物的物质的量之比。图中表示平衡转化率的曲线是(填“a”“b”或“c”),其如图变化的原因是。
选项 | 实验操作 | 现象 | 结论 |
A | 将 | 产生浅黄色沉淀 |
|
B | 向2mL0.1 | 产生红褐色沉淀 | |
C | 将盛有2mL0.5 溶液的试管,先加热,后冷却 | 加热时蓝绿色溶液变为黄绿色,冷却后恢复为蓝绿色 | 反应 |
D | 加热试管中的聚氯乙烯薄膜碎片 | 试管口润湿的蓝色石蕊试纸变红 | 氯乙烯加聚铈可逆反应 |

已知:①;
②焦亚硫酸钠()常用作食品抗氧化剂;
③氧化性:。
回答下列问题:
a.CoO
b.
c.KOH


选项 | 实验操作及现象 | 结论 |
A | 向重铬酸钾溶液中加水,溶液颜色变浅 | 增加水的用量,平衡 |
B | 向含酚酞的 |
|
C | 向硫酸铜溶液中滴加浓氨水至过量,溶液先产生蓝色沉淀,然后沉淀溶解变为深蓝色溶液 |
|
D |
|
|