选项 | 探究方案 | 探究目的 |
A | 将 |
|
B | 将 |
|
C | 向饱和 | 比较 |
D | 向 | 比较 |

| 实验方案 | 现象 | 结论 |
A |
| 出现乳白色浑浊,产生气体 | 生成硫单质,不能证明 |
B | 将铜丝放入浓硫酸中,加热 | 开始时铜丝表面变黑,产生无色气体,后黑色固体溶解 | 由氧化还原规律可知黑色固体一定是 |
C | 久置于空气中的 | 出现乳白色浑浊 |
|
D | 0.5g硫粉和1.0g铁粉混合均匀,在石棉网上堆成条状,用灼热的玻璃棒接触混合粉末的一段 | 粉末呈红热状态,持续反应,冷却后得到黑色固体 | 硫粉与铁粉接触面积大,反应放热,生成黑色 |
选项 | 实验操作 | 实验目的 |
A | 向某未知溶液中加入一定量的BaCl2溶液 | 检验该溶液中是否含有 |
B | 将含有NO2杂质的NO气体通过足量水和浓硫酸 | 提纯NO气体 |
C | 在碳酸钙中滴加浓硝酸,并将产生的气体通入硅酸钠溶液 | 证明非金属性:N>C>Si |
D | 将SO2和CO2分别通入澄清石灰水中 | 区别CO2和SO2气体 |


 实验②中Cu溶解的离子方程式为。实验②产生的气体为,产生该气体的原因为。
实验②中Cu溶解的离子方程式为。实验②产生的气体为,产生该气体的原因为。
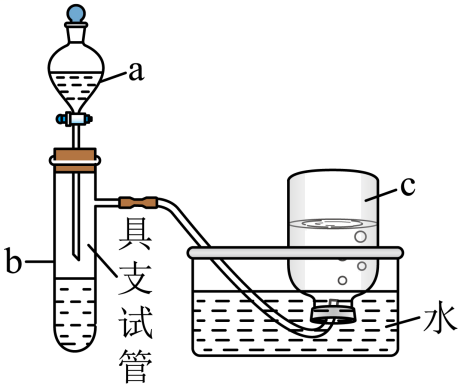
将铜片置于具支试管的底部,在分液漏斗中加入约5mL浓硝酸,往具支试管中放入约2mL浓硝酸,集气瓶c中收集到一种无色气体。
仪器a的名称为。上述反应完成后,欲进一步证明稀硝酸也具有强氧化性,可以将浓硝酸稀释后加入具支试管再与铜片反应,此时发生反应的离子方程式是;集气瓶c中仍收集到一种无色气体,此时向集气瓶c中通入一定量的氧气后集气瓶c中逐渐充满无色溶液,请写出通入一定量的氧气后集气瓶c中发生的总反应方程式。
用等质量铜片与等体积的浓硝酸、稀硝酸(硝酸均过量)反应时,发现反应后所得溶液前者呈绿色,后者呈蓝色。对此有两种看法:
①两者颜色不同的原因,是因为Cu2+浓度差异引起的。
②前者溶液呈绿色,是因为生成的红棕色NO2溶解于溶液中引起的。
你认为上述看法(填“①”或“②”)合理。若是①合理,说明理由,若是②合理,设计一个简单实验证明:。
选项 | 猜想 | 实验方案 | 验证猜想成立的现象 |
A | 苯酚能与 | 向苯酚浊液中加入适量 | 苯酚浊液变澄清 |
B | 某溶液中一定含有 | 取少量该溶液,先滴加少量 | 产生白色沉淀且沉淀不溶于稀盐酸 |
C | 加热条件下 | 将灼热的铜丝插入无水乙醇中 | 铜丝由红色变成黑色 |
D | 浓 | 向滴有酚酞的NaOH溶液中加入浓 | 溶液红色褪去 |