。(电负性:
)
下列说法正确的是。
A.原子半径:
B.GaAs为共价晶体,为分子晶体
C.沸点:
D.化学键中离子键成分的百分数:
②比较键角:
中的
中的
(填“>”“<”或“=”),请说明理由

如图所示晶胞沿着z轴的投影图为(填选项字母)。
A.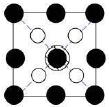 B.
B. C.
C.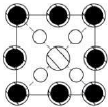 D.
D.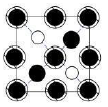
化合物 | ||||
熔点/℃ | 377 | 38.3 | 155 |
元素代号 | 元素的性质或原子结构 |
Q | 有一种原子不含中子 |
W | M层上的电子数为4 |
X | 常温下单质为双原子分子,其简单氢化物的水溶液显碱性 |
Y | L层的电子数为次外层电子数的3倍 |
Z | 元素的最高化合价是 |
下列叙述中错误的是( )



①的离子结构示意图为。
②表中几种元素的最高价氧化物对应水化物酸性最强的是(填化学式);写出该物质在水溶液中的电离方程式:。
③用电子式表示短周期元素中,原子半径最大的元素与氯形成的简单化合物的形成过程:。
④氰是一种无色、可燃气体,剧毒、有苦杏仁味,与卤素单质
![]() 性质相似,试写出氰与NaOH溶液在常温下反应的离子方程式:。
性质相似,试写出氰与NaOH溶液在常温下反应的离子方程式:。
①写出Se在周期表中的位置:。
②溶于水生成
, 向所得溶液中通入
气体发生反应,生成Se和
。写出
与
反应的化学方程式:。
a.原子半径:
b.中存在的化学键为非极性共价键
c.非金属性:Cl>Se>Br