①恒容条件下,再通入一定量的NH3 ②增大体系容积③恒容条件下,再通入一定量的N2 ④适当升高温度
a.容器的体积保持不变
b.二氧化碳的浓度保持不变
C.CH3OH的百分含量保持不变
d.化学反应速率3v正(H2)=v逆(CH3OH)

回答下列问题:

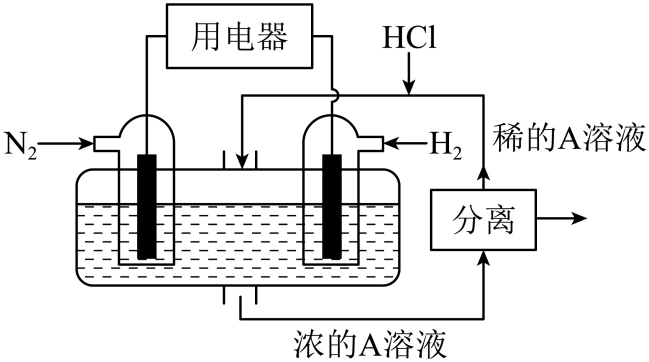
①A化学式为。
②电池正极的电极反应式为。
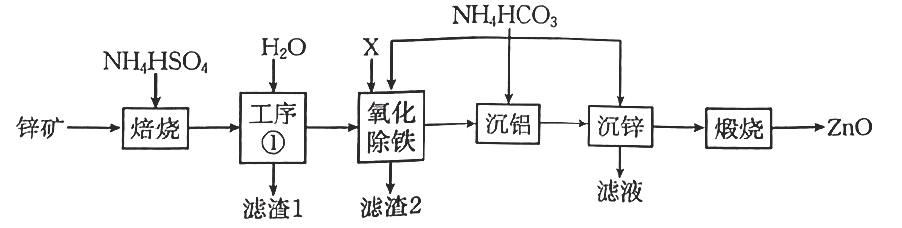
已知:①“焙烧”时金属元素生成硫酸盐。
②下,
的
的
,
的
。
③当离子浓度时,可视为沉淀完全。
回答下列问题:
②。
则③中的
(用含
的式子表示),
(用含
的式子表示),该反应中每消耗
, 此时转移的电子数为
。
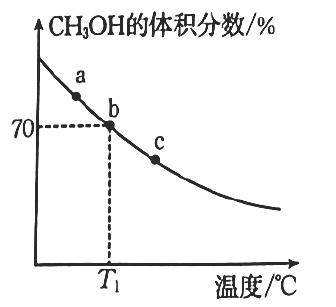
①下列有关反应的说法正确的是(填标号)。
A.该反应的反应物的键能总和小于生成物的键能总和
B.当混合气体的密度不再随时间改变时,该反应达到平衡
C.升高温度,有利于增大的平衡转化率
D.无论反应进行到何种程度,为某一定值
②平衡常数由大到小的顺序为。
③反应速率:(填“>”“<”或“=”)
。
④ , b点的平衡常数
。
ⅰ.
ⅱ.
ⅲ.
热分解反应
的
(用含
、
、
的式子表示)。
ⅳ.
ⅴ.
根据以上络合反应,下列说法正确的有____(填字母)。

①时,图中含铬微粒按浓度由大到小的顺序为;A点时,溶液中
的平衡浓度为(列出计算式即可)。
②在某电镀工艺中,的浓度需要在
以上,结合计算判断C点所对应的溶液能否用于该电镀工艺(写出计算过程)。