①当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是。
②若三者c(H+)相同时,物质的量浓度由大到小的顺序是。

酸 | 电离平衡常数 |
醋酸 | |
碳酸 |
|
亚硫酸 |
|

a.溶液的pH b.醋酸的电离平衡常数
c.溶液的导电能力 d.醋酸的电离程度
Ka2
Kh2(水解平衡常数,表示水解程度)
已知25 ℃时,Ka2 > Kh2 , 则0.1 mol∙L−1 NaHSO3溶液呈(填“酸性”“碱性”或“中性”);其中c(Na+)c()(填“>”“<”或“=”);其电荷守恒表达式可写为。
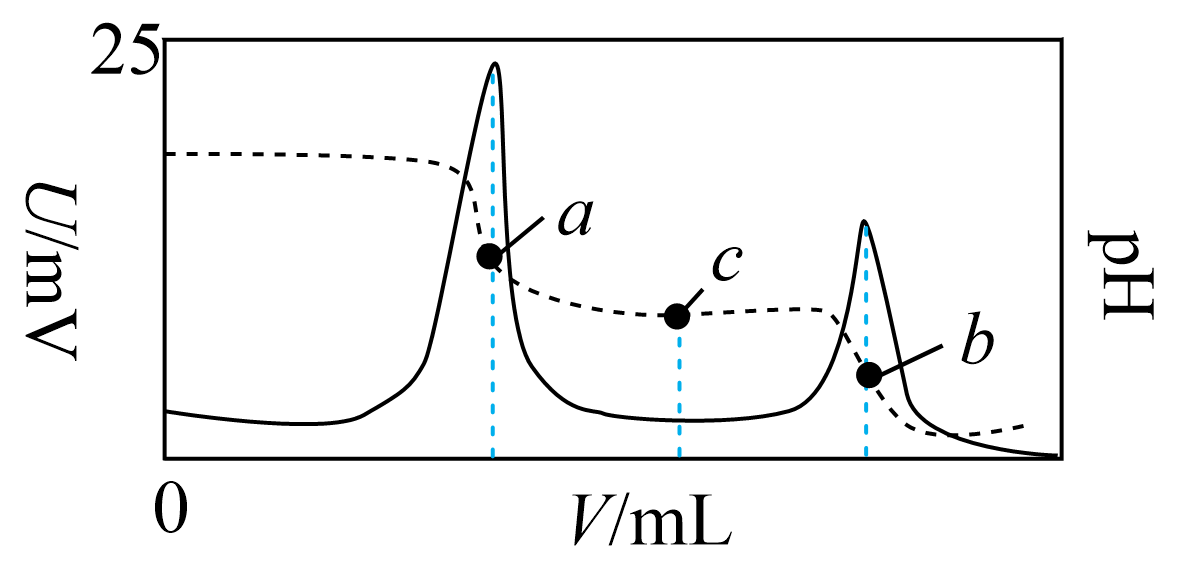
[已知:①电位滴定法的原理:在化学计量点附近,被测离子浓度发生突跃,指示电极电位也发生了突跃,进而确定滴定终点。②亚磷酸是二元弱酸,其电离常数分别是
,
]
金属离子 | |||
开始沉淀时的 | 6.3 | 2.2 | 8.9 |
完全沉淀时的 | 9.0 | 2.8 | 10.9 |
上述流程中所用“氧化剂”常用双氧水,这一步不可省掉的理由是。