


①盐酸的浓度 ②镁条的表面积 ③溶液的温度 ④Cl-的浓度


该反应是(填“放热”或“吸热”)反应,反应在(填“低温”或“高温”)下能自发进行。
平衡时,若、
与
三者的物质的量相等,则
转化率为,反应
平衡常数
(用含p的代数式表示)。
①
②
,
。
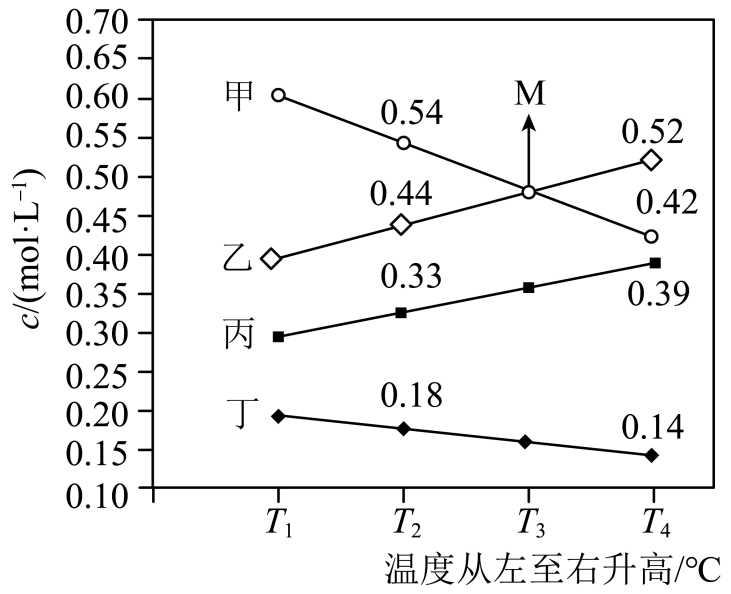
①甲是(填化学式),写出该反应的化学方程式:。
②正反应(填“>”“<”或“=”)0,判断依据是
③T3℃时NH3的平衡转化率为。
化学键 | C=O | H—O | H—H | C—O | C—H | C—C |
键能( | 803 | 463 | 436 | 326 | 414 | 348 |
依据表中数据计算的
H=
, 下列有利于该反应自发进行的条件是(填标号)。
A.高温 B.低温 C.任何温度

该反应中形成的化学键有____(填标号)。
a. b.容器中气体的平均摩尔质量不变
c.CH3CH2OH的百分含量保持不变 d.容器中混合气体的密度保持不变

①表示的曲线为(填标号)。
②、
、
由大到小的顺序是。
③℃、投料比为
下,该反应的平衡常数
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
温度/℃ | 220 | 240 | 250 | 255 |
BL/% | 60.2 | 84.6 | 92.6 | 95.2 |
| 1.2 | 1.8 | 1.9 | 2.1 |
| 0.2 | 0.3 | 0.4 | 0.6 |
已知:![]()
下列说法不正确的是( )