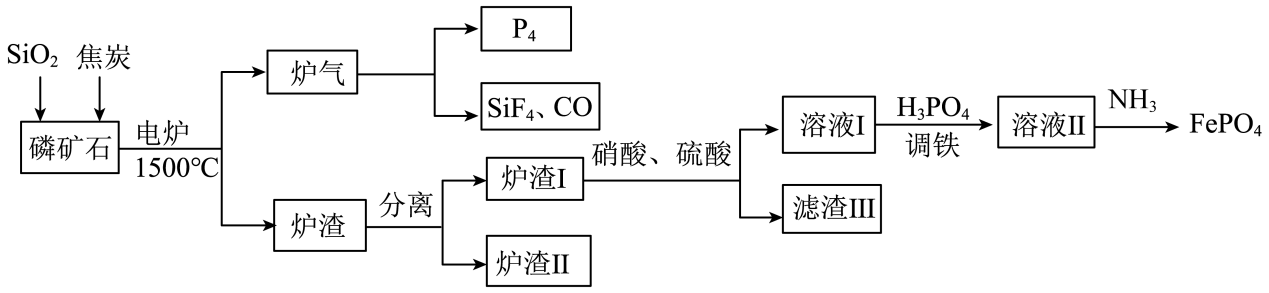
已知:①FePO4可溶于pH<2的酸性溶液。
②Fe3+在pH为2.0时开始沉淀,pH为4.0时沉淀完全。
回答下列问题:
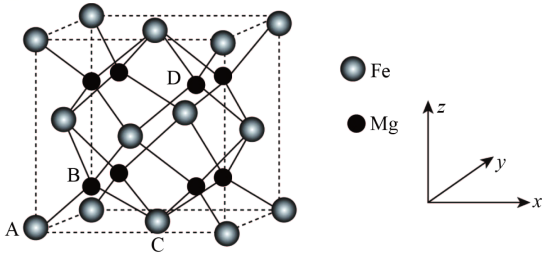
其中A的原子坐标参数为(0,0,0), B为( ,
,
),C为(
,
, 0),则D点的坐标参数为。此晶胞中Fe的配位数是。

①加热反应前通的目的是。
②A中仪器X的名称是,其作用是。
③E中收集的物质含有(写化学式)。
④尾气经处理后可循环使用。
①中存在的化学键有(填序号)。
a.配位键 b.氢键 c.离子键 d.金属键
②该暗绿色晶体的化学式为。
选项 | 实验目的 | 实验方案 |
A | 探究葡萄糖的还原性 | 在一支试管中先加入2mL10%NaOH溶液,滴入5滴5%CuSO4溶液,再加入2mL10%葡萄糖溶液,加热。观察实验现象 |
B | 检验苯中是否含有苯酚 | 在盛有苯和苯酚混合溶液的试管中滴加少量溴水。观察实验现象 |
C | 探究不同盐的水解程度 | 用pH试纸分别测量等体积、等浓度的NaClO溶液和CH3COONa溶液的pH。比较大小 |
D | 检验乙烯的还原性 | 在圆底烧瓶中加入乙醇和浓硫酸的混合溶液,并加入碎瓷片,迅速升温到170℃,将生成的气体通入高锰酸钾溶液中。观察实验现象 |