选项 | 物质性质 | 结构因素 |
A | 乙醇与钠的反应没有水与钠的反应剧烈 | 氢氧键极性 |
B | 对羟基苯甲酸的沸点高于邻羟基苯甲酸 | 氢键类型 |
C | 干冰因易升华而用作制冷剂 | 共价键强弱 |
D | 水晶柱面上的固态石蜡在不同方向熔化的快慢不同 | 原子有序排列 |

写出电解槽中阴极反应式。
化学键 | ||||
键能/( | 348 | 615 | 413 | 436 |


①表示的曲线为(填“M”或“N”)。
②a点反应的平衡常数kPa(列出计算式,分压=总压×物质的量分数)。

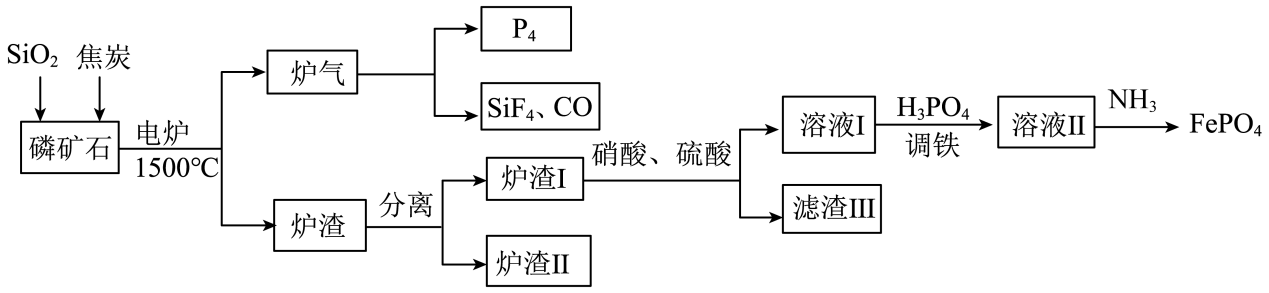
已知:①FePO4可溶于pH<2的酸性溶液。
②Fe3+在pH为2.0时开始沉淀,pH为4.0时沉淀完全。
回答下列问题:
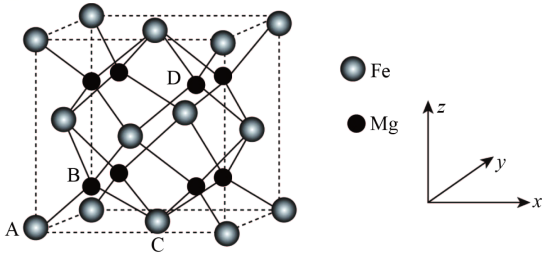
其中A的原子坐标参数为(0,0,0), B为( ,
,
),C为(
,
, 0),则D点的坐标参数为。此晶胞中Fe的配位数是。

已知:GeO2可溶于强碱溶液,生成锗酸盐;GeCl4的熔点为-49.5℃,沸点为84℃,在水中或酸的稀溶液中易水解。
编号 | 加料量(CaCl2/Ge) | 母液体积(mL) | 过滤后滤液含锗(mg/L) | 过滤后滤液pH | 锗沉淀率(%) |
1 | 10 | 500 | 76 | 8 | 93.67 |
2 | 15 | 500 | 20 | 8 | 98.15 |
3 | 20 | 500 | 2 | 11 | 99.78 |
4 | 25 | 500 | 1.5 | 12 | 99.85 |
①量子化学计算显示含锗化合物H5O2Ge(BH4)3具有良好的光电化学性能。CaPbI3是H5O2Ge(BH4)3的量子化学计算模型,CaPbI3的晶体结构如图所示,若设定图中体心钙离子的分数坐标为( ,
,
),则分数坐标为(0,0,
)的离子是。

②晶体Ge是优良的半导体,可作高频率电流的检波和交流电的整流用。如图为Ge单晶的晶胞,设Ge原子半径为rpm,阿伏加德罗常数的值为NA , 则该锗晶体的密度计算式为(不需化简)ρ=g/cm3。


①综合分析,反应的最佳温度的范围为(填标号)。
A. B.
C.
左右
②随着温度的升高,环戊二烯转化率升高而环戊烯选择性降低,其原因是。

①中Fe3+的杂化轨道类型为(填字母)。
A. B.
C.
D.
②配体SCN-和H2O的键角大小:SCN- H2O (填“<”“>”或“=”。用杂化轨道理论解释,其原因为。
③SCN-中所有原子均满足最外层8电子结构。写出SCN-的电子式。

①以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的相对位置,称作原子坐标。如1号原子的坐标为 , 2号原子的坐标为
, 则3号Fe原子的坐标为。
②若晶胞参数分别为apm、bpm、cpm,阿伏加德罗常数的值为NA , 则晶体的密度为 g∙cm-3 (列出计算表达式)。


已知:。