选项 | 实验目的 | 实验方案 |
A | 探究葡萄糖的还原性 | 在一支试管中先加入2mL10%NaOH溶液,滴入5滴5%CuSO4溶液,再加入2mL10%葡萄糖溶液,加热。观察实验现象 |
B | 检验苯中是否含有苯酚 | 在盛有苯和苯酚混合溶液的试管中滴加少量溴水。观察实验现象 |
C | 探究不同盐的水解程度 | 用pH试纸分别测量等体积、等浓度的NaClO溶液和CH3COONa溶液的pH。比较大小 |
D | 检验乙烯的还原性 | 在圆底烧瓶中加入乙醇和浓硫酸的混合溶液,并加入碎瓷片,迅速升温到170℃,将生成的气体通入高锰酸钾溶液中。观察实验现象 |
连接仪器后,装入药品前,应进行的操作是。
移去装置A处的酒精灯,关闭K1 , 打开K2 , 利用分液漏斗边加液边加热,则此时装置D中发生反应的化学方程式是。用橡皮管连接三颈烧瓶和分液漏斗的作用是。
称取10.00g样品配成1L溶液,量取25.00mL溶液于锥形瓶中,并加入几滴Fe(NO3)3溶液,用0.1000mol·L-1AgNO3标准溶液滴定。经过3次平行试验,达到滴定终点时,消耗AgNO3标准溶液的体积平均为20.00mL。滴定反应的离子方程式为SCN-+Ag+=AgSCN↓。
滴定管读数时,平视观察的位置为。

Ti元素在周期表中的位置是。

M电极为极(填“正”或“负”),该电极反应方程式为。
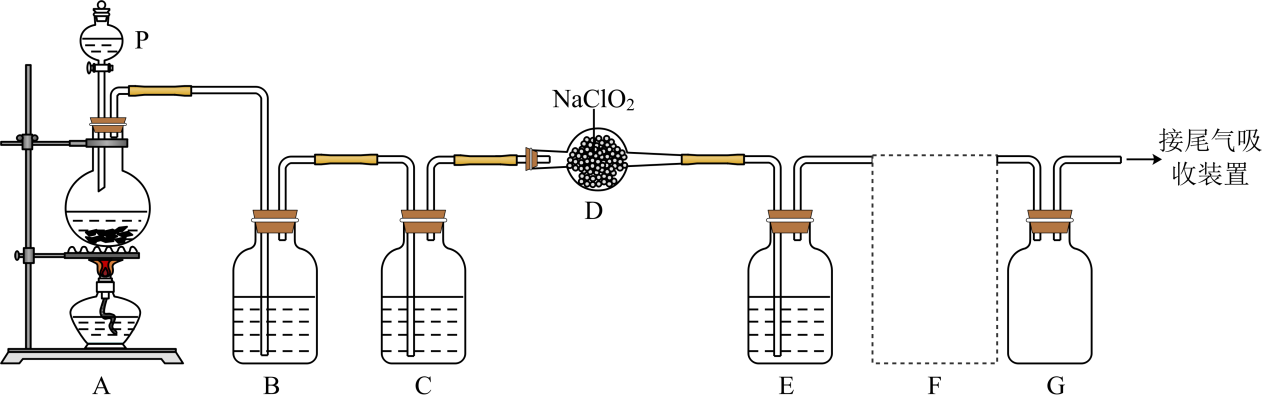
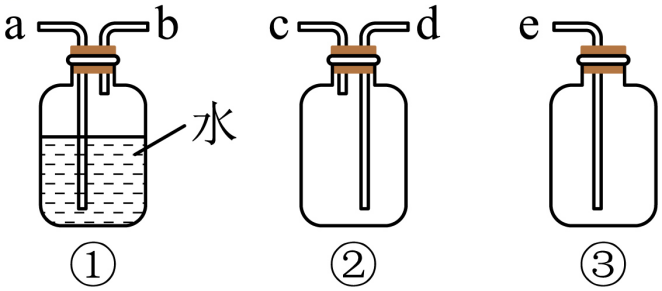
①请写出该反应的化学方程式:,每消耗319.5gNaClO3 , 生成L氯气(标况下)。(M(NaClO3)=106.5)。
②浓盐酸在该反应中表现出来的性质是(填序号)。
A. 只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
实验方案 | 现象 | 结论 | |
A |
| 出现乳白色浑浊,产生气体 | 生成硫单质,不能证明 |
B | 将铜丝放入浓硫酸中,加热 | 开始时铜丝表面变黑,产生无色气体,后黑色固体溶解 | 由氧化还原规律可知黑色固体一定是 |
C | 久置于空气中的 | 出现乳白色浑浊 |
|
D | 0.5g硫粉和1.0g铁粉混合均匀,在石棉网上堆成条状,用灼热的玻璃棒接触混合粉末的一段 | 粉末呈红热状态,持续反应,冷却后得到黑色固体 | 硫粉与铁粉接触面积大,反应放热,生成黑色 |
