选项 | 陈述Ⅰ | 陈述Ⅱ |
A | 淀粉水解产生果糖 | 米饭在口腔中越嚼越甜 |
B |
| 加热可除去 |
C | Zn的金属性比Fe强 | 在钢制船壳上镶嵌锌块能减缓船体的腐蚀 |
D |
| 工业上电解熔融 |
①验证该混合溶液中含有的方法及现象为。
②NaOH中存在的化学键为。
③将少量的氧化铝投入该混合溶液中,发生反应的化学方程式为。
选项 | 劳动项目 | 化学知识 |
A | 社区服务:草坪施肥 |
|
B | 家务劳动:柠檬煮水除去水壶中的水垢 | 柠檬酸可溶解碳酸钙等沉淀 |
C | 趣味实验:用铝粉和氢氧化钠溶液疏通厨卫管道 | 铝粉与 |
D | 学农活动:用厨余垃圾制肥料 | 厨余垃圾含N、P等元素 |
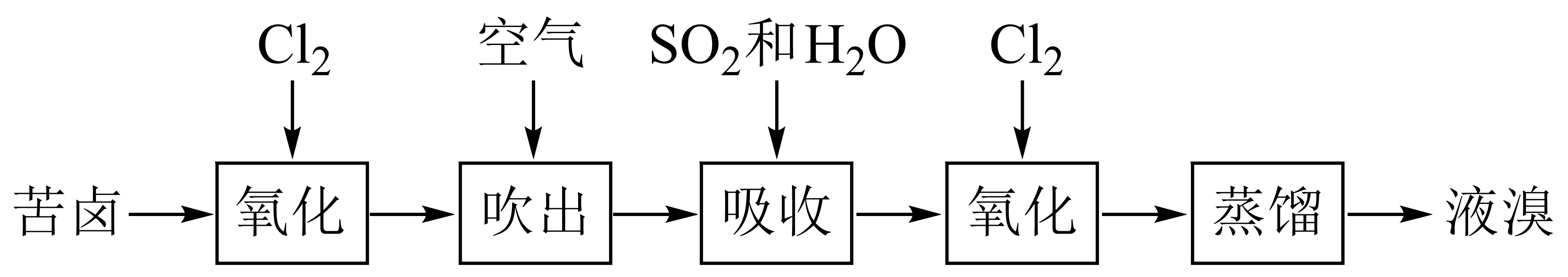
以苦卤为原料提Br2而不是直接利用海水提Br2 , 优势在于。
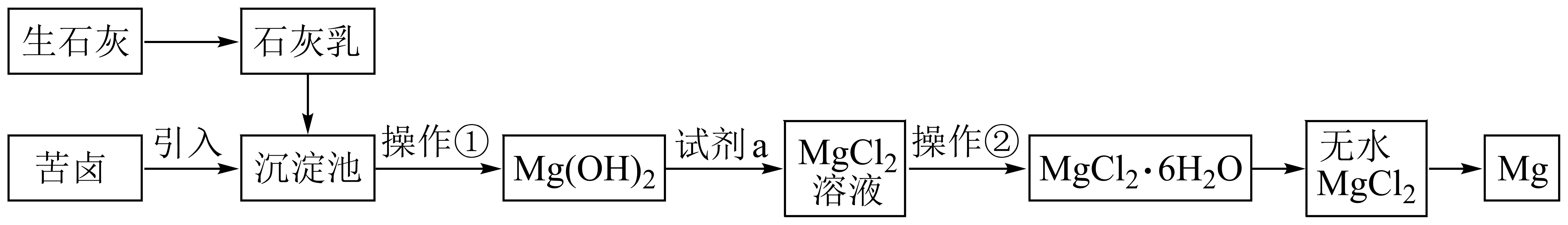
已知:MgO的熔点为2852℃,无水MgCl2的熔点为714℃。
沉淀池中发生主要反应的离子方程式为。
a.N2 b.Ar c.CO2 d.O2
A. B.
C.
D.