| 物质m | 物质n | 现象推测 | 原理分析 |
① | 稀硫酸 | 锌粉 | 逐渐鼓起并保持 | Zn+H2SO4═ZnSO4+H2↑ 反应产生气体,内压保持不变 |
② | 水 | 硝酸铵固体 | 逐渐变瘪并保持 | 硝酸铵溶于水,温度降低,内压减小并保持 |
③ | 氢氧化钠溶液 | 二氧化碳 | 逐渐变瘪并保持 | 2NaOH+CO2═Na2CO3+H2O 反应消耗气体,内压减小并保持 |
④ | 水 | 生石灰 | 逐渐鼓起,慢慢恢复 | CaO+H2O═Ca(OH)2反应放热,温度升高,反应结束一段时间后恢复常温,内压先增大后恢复 |

氢能是一种清洁能源,氢气的生产和储存是科学研究的重要方向。
目前制氢的方法主要有化石能源制氢、电解水制氢和乙醇裂解制氢等。由化石能源制得的H2中含有CO,利用液氮的低温可将CO液化分离,从而获得纯净的H2.电解法制氢的能量转化如图1所示,其中利用可再生能源制得的氢气称为绿色氢气。乙醇裂解制氢会受到反应温度、催化剂种类等多种因素的影响。图2为我国科研人员研究反应温度对Ni/C催化裂解乙醇产氢率的影响。

氢气的储存方法有物理储氢和化学储氢。中国科学家研究出镁基固态储氢技术:利用金属镁和氢气在300℃和高压条件下发生反应生成氢化镁(MgH2),实现了固态储氢。MgH2是氢能源汽车的供能剂,它能与水反应生成氢氧化镁,同时释放出氢气。氢能源能有效减少CO2的排放,随着制氢与储氢技术的不断发展,氢能源作为一种理想的清洁能源,其发展前景可期。
依据文章内容回答下列问题。
①利用太阳能发电并电解水制氢可实现CO2零排放
②由图2可知,温度越低,Ni/C催化裂解乙醇产氢率越大
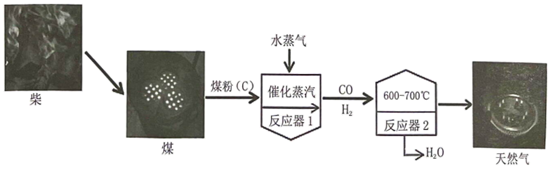
①在催化剂和高温的条件下,C(即煤粉)与H2O发生反应生成CO和H2 , 该反应的化学方程式为;属于反应(填基本反应类型),反应物中具有还原性的物质是(填化学式)。
②反应器2:600-700℃时,CO与H2发生反应生成甲烷和水,参与反应的CO与H2的分子个数比为。
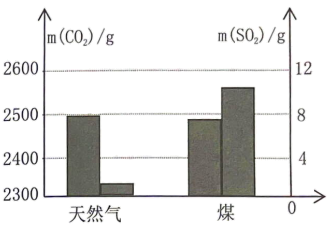
随者工业生产的高速发展和人们生活水平的提高,排入大气中的CO2越来越多,导致温室效应增强。碳替代、碳减排、碳封存、碳循环是实现碳中和的4种主要途径。
科学家预测,到2050年,4种途径对全球碳中和的贡献率如图1所示。CO2的吸收是碳封存的首要环节,常选用NaOH溶液、氨水、一乙醇胺等作吸收剂。在研究膜吸收法吸收CO2时,研究人员通过实验比较了氨基乙酸钾、一乙醇胺、二乙醇胺3种吸收剂对烟气中CO2的脱除效果,其结果如图2所示。
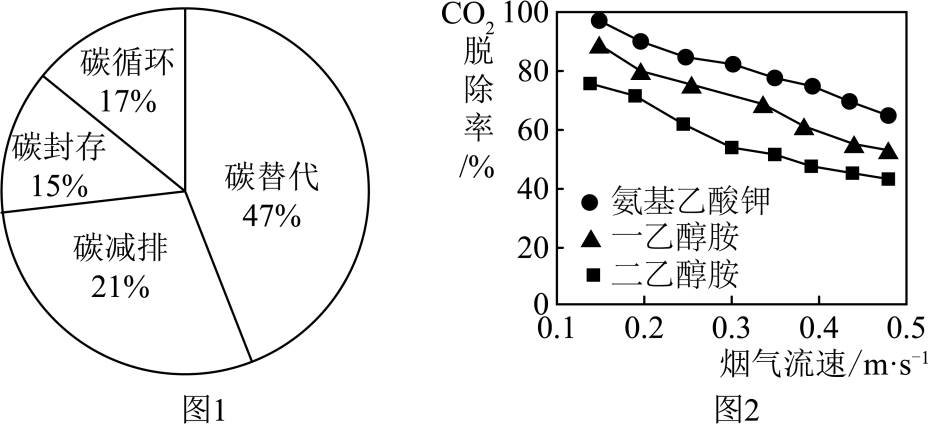
依据上文,回答下列问题