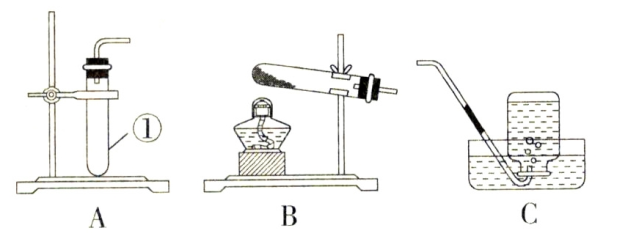

第一步:2Na2CO3•3H2O2═2Na2CO3+3H2O2
第二步:产生氧气的化学方程式为 。
物质m | 物质n | 现象推测 | 原理分析 | |
① | 稀硫酸 | 锌粉 | 逐渐鼓起并保持 | Zn+H2SO4═ZnSO4+H2↑ 反应产生气体,内压保持不变 |
② | 水 | 硝酸铵固体 | 逐渐变瘪并保持 | 硝酸铵溶于水,温度降低,内压减小并保持 |
③ | 氢氧化钠溶液 | 二氧化碳 | 逐渐变瘪并保持 | 2NaOH+CO2═Na2CO3+H2O 反应消耗气体,内压减小并保持 |
④ | 水 | 生石灰 | 逐渐鼓起,慢慢恢复 | CaO+H2O═Ca(OH)2反应放热,温度升高,反应结束一段时间后恢复常温,内压先增大后恢复 |

选项 | 实验目的 | 实验设计 |
A | 鉴别稀盐酸和稀硫酸 | 分别滴加Na2CO3溶液 |
B | 除去铁粉中混有的少量碳粉 | 加入足量的稀硫酸,过滤 |
C | 鉴别羊毛和合成纤维 | 取样灼烧,闻气味 |
D | 除去KNO3溶液中AgNO3 | 先加入过量KCl溶液,再过滤 |
生活中:用干冰(固体CO2)对生鱼片保鲜,利用了干冰升华(填“吸热”或“放热”)的原理。
①生产化肥:合成尿素的反应为 , x的化学式是。
②催化重整转化成较清洁的燃料:CH4与CO2在催化剂作用下可得到合成气(CO和H2),反应过程中催化剂表面还同时存在积碳反应和消碳反应,原理如图1所示。
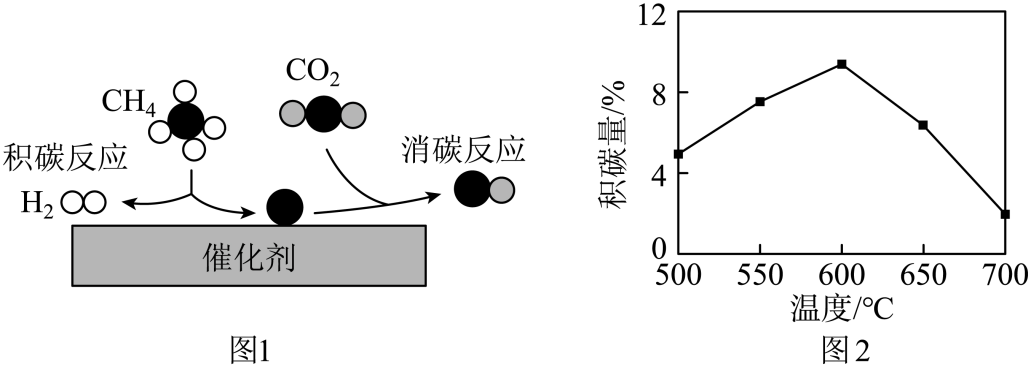
a.消碳反应的产物“![]() ”是。
”是。
b.为减少催化剂表面的积碳,可在原料气中加入适量气体。
c.其他条件不变,催化剂表面的积碳量随温度变化如图2所示。温度高于600℃,催化剂表面积碳量减少的原因可能是。
