
回答下列问题:
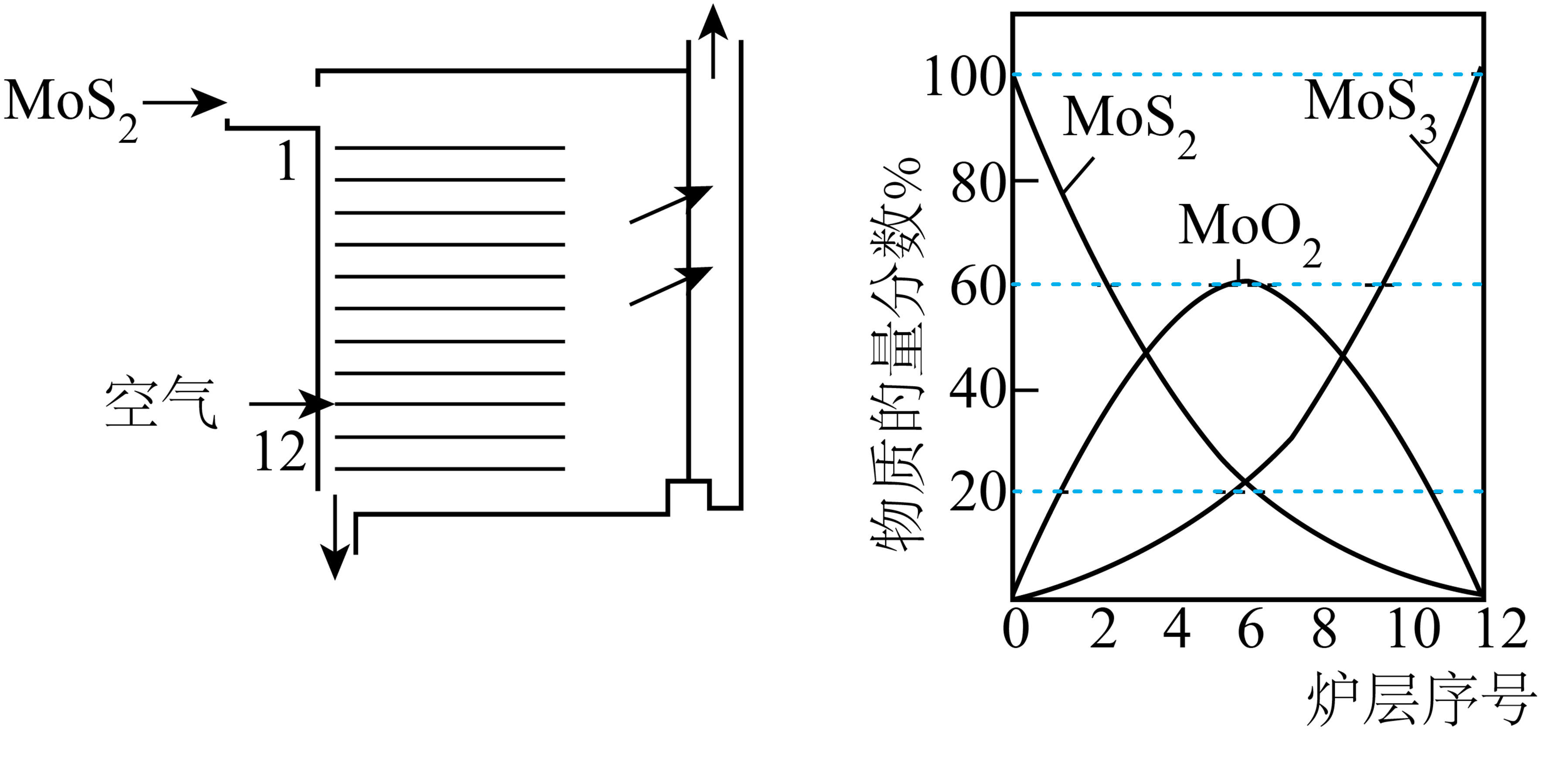
①多层逆流焙烧的优点是(任答一点)。
②固体1的成分有、CuO和Fe2O3。

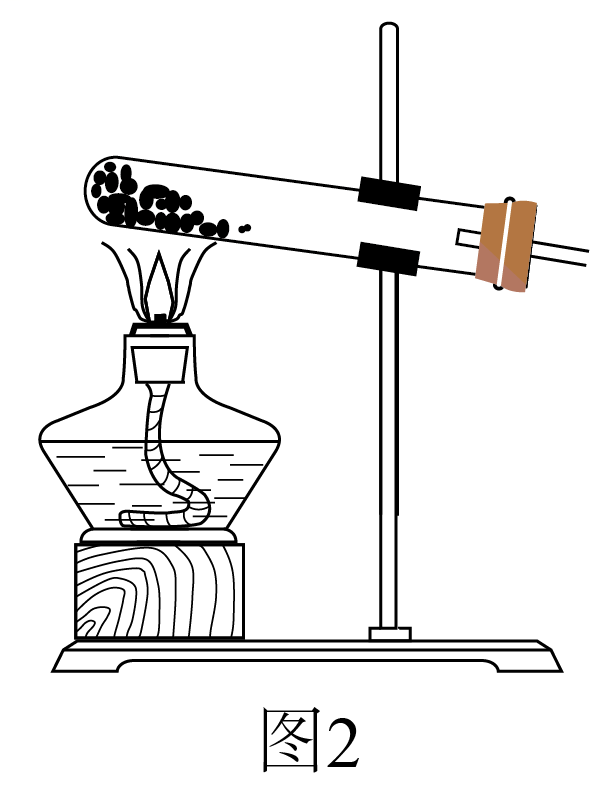
①简述使用分液漏斗向圆底烧瓶中滴加浓硫酸的操作:。
②实验过程中,需要通入氧气。试写出一个用如图2所示装置制取氧气的化学方程式:。
③当停止通入SO2熄灭酒精灯后,需要继续通一段时间的氧气,其目的是:。
④实验结束后,若装置D增加的质量为mg,装置E中产生白色沉淀的质量为ng,则此
条件下二氧化硫的转化率是(用含字母的代数式表示,不用化简)。
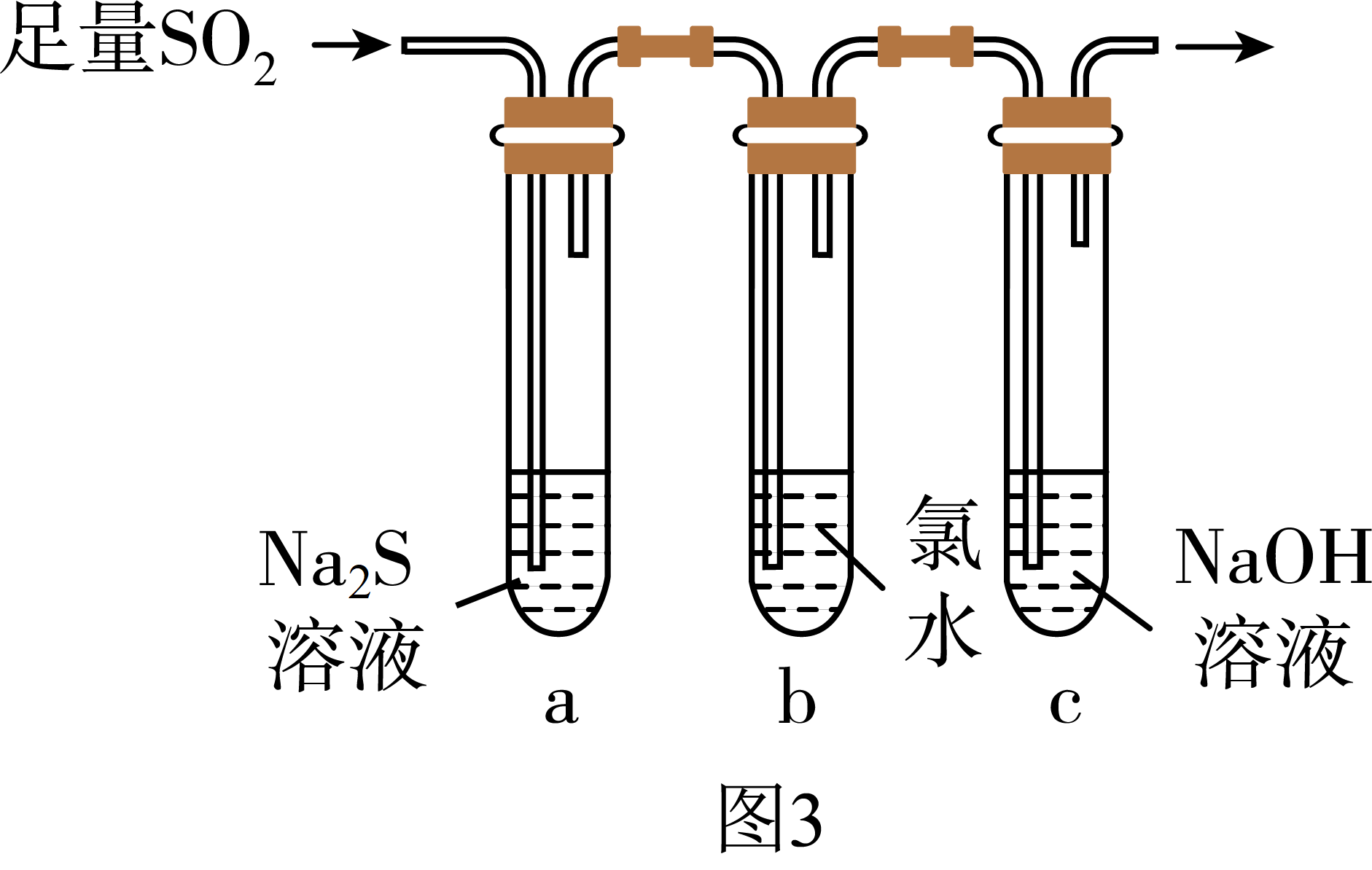
①能说明二氧化硫具有氧化性的实验现象为: 。
②为验证二氧化硫的还原性,充分反应后,取试管b中的溶液分三份,分别进行如下实验。
方案I:向第一份溶液中加入AgNO3溶液,有白色沉
淀生成。
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去。
方案Ⅲ:向第三份溶液中加入BaCl2溶液,产生白色沉淀
上述方案中合理的是 (填“I”、“Ⅱ”、或“Ⅲ”);
试管b发生反应的离子方程式:。
③当通入二氧化硫至试管c中溶液显中性时,该溶液中
c(Na+)=用含硫微粒浓度的代数式表示)。

已知:i.水溶液中不存在碳酸铜,碳酸铜遇水立即水解为碱式碳酸铜和氢氧化铜。
ii.室温时,的溶度积常数
。
ⅰ.组装好装置,检验装置气密性,向瓷舟中加入。
ⅱ.向体系中通入干燥纯净的一段时间。
ⅲ.使通过
, 进入到硬质玻璃管中,同时打开管式炉,对反应物加热。
ⅳ.制备实验结束后,继续通入纯净的 , 直至产物冷却为室温,硬质玻璃管右端有紫色薄片出现。
ⅴ.检测产品纯度。
实验装置如图所示:

已知相关部分物质的性质如下表:
无水氯化铬( | 紫色晶体,950℃升华,易溶于水 |
绿色粉末固体,熔点2435℃,高温下能被 | |
无色液体,沸点:76~77℃ | |
光气( | 无色气体,剧毒,遇水水解: |
回答下列问题: