

选项 | 实验操作 | 实验现象 | 实验结论 |
A | 向蔗糖溶液中加入稀硫酸煮沸,冷却,加入银氨溶液,水浴加热 | 无银镜产生 | 说明蔗糖的水解产物中无葡萄糖 |
B | 常温下,将苯酚和NaOH溶液混合(已知:苯酚 | 用pH计测得混合液的pH=10.0 | 混合液中: |
C | 向溶液中滴加硝酸,再滴加 | 有白色沉淀生成 | 溶液中一定含有 |
D | 将Ag和 | Ag电极表面有银白色金属沉积,Cu电极附近溶液变蓝 | 金属性:Cu>Ag |
①在三组100mL12mg•L-1的B溶液中分别加入0.075gHgO,在不同波长的可见光照射下做光催化活性测试,溶液中某时刻B的浓度c与初始浓度c0的比值随光照时间t的变化如下图所示,三条曲线产生差异的原因可能是。

②0~15min内,470nm可见光照射下B的降解速率为mg•L-1•min-1。

①从上图可知,CH2=CHOH(aq)→CH3CHO(aq) ∆H=(用相对能量E表示)。
②下列说法正确的是。
A.本反应历程涉及的物质中,CH2=CHOH最不稳定
B.过程①中,Hg2+的空轨道接受水分子中氧原子的孤对电子
C.该反应历程中,存在非极性键的断裂和形成
D.增大压强和乙炔的浓度均能加快反应速率,并且增大乙炔的平衡转化率
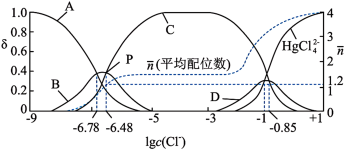
已知:平均配位数
①图中能代表HgCl2曲线是(填字母),平衡常数K4=。
②在P点,溶液中c(HgCl2):c(Hg2+)=(写出计算过程)。

已知:①CeO2不溶于稀硫酸,也不溶于NaOH溶液;②常温下Ksp[Fe(OH)2]=4.0×10-16 , Ksp[Fe(OH)3]=8.0×10-38 , Ksp[Al(OH)3]=3.0×10-33 , lg2=0.3。
回答下列问题:

实验序号 | 操作 | 现象 | |
实验i:[Cu(NH3)4]2+的配制 | 实验i-a | 在试管内混合CuSO4溶液和NaOH溶液,再加入过量的2mol/LNH3·H2O | 产生蓝色沉淀,加入NH3·H2O后沉淀少部分溶解,溶液变浑浊,静置后上层为深蓝色溶液。 |
实验i-b | 在试管内混合CuSO4溶液和NaOH溶液,再加入过量的6mol/LNH3·H2O | 产生蓝色沉淀,加入NH3·H2O后沉淀大部分溶解,溶液变浑浊,静置后上层为深蓝色溶液。 | |
实验i-c | 在试管内混合CuSO4溶液和NH3·H2O溶液,再加入过量的2mol/LNH3·H2O | 产生蓝色沉淀,加入NH3·H2O后沉淀完全溶解,得到澄清的深蓝色溶液。 | |
实验ii:[Co(NH3)6]2+的配制 | 实验ii-a | 在试管内混合CoCl2溶液和过量6mol/LNH3·H2O | 得到浅青色沉淀,沉淀未见明显溶解。 |
实验ii-b | 在试管内混合CoCl2溶液和过量14mol/LNH3·H2O | 得到浅青色沉淀,沉淀未见明显溶解。 | |
资料:①Co(OH)2为浅青色沉淀
②[Co(NH3)6]2+溶液为红色,在活性炭催化下转化为橙黄色的[Co(NH3)6]3+溶液

①在实验ii-a的基础上继续加入,即可成功配制。
②验证配制成功![]() 操作及实验现象是:;反应的离子方程式为:。
操作及实验现象是:;反应的离子方程式为:。