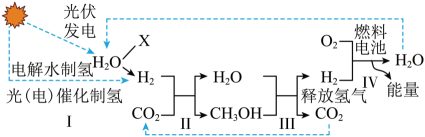
;往试管中加入氯酸钾粉末的操作是。
若要制得较纯净的氧气应选择的装置组合是(填字母序号),当时开始收集氧气。

[提出问题]蔗糖的组成元素有哪些?
[查阅资料]①蔗糖受热时会发生分解反应;
②铜可以和氧气加热后反应会生成氧化铜。.
[进行实验]兴趣小组成员进行了下述两种不同的实验方案:

实验步骤 | 实验现象 | 实验结论 |
打开甲仪器的活塞: 待排尽装置中空气后,加热蔗糖。 | b中玻璃管右端有小液滴产生,c中现象是 (此处不用填写,在后文作答) | 蔗糖在氧气中加热,生成水和二氧化碳。 |
实验二(如图2)
实验步骤 | 实验现象 | 实验结论 |
先用酒精灯加热铜丝处,并反复推拉注射器活塞; 再将酒精灯移置蔗糖处加热 | 铜丝表面生成 色的物质,蔗糖固体变少,玻璃管右侧端有小液滴生成。 (此处不用填写,在后文作答) | 蔗糖受热分解,其中一种生成物是水。 |
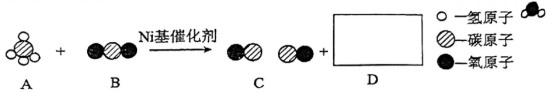
根据质量守恒定律,化学变化前后,元素种类 (填 “变多”、“变少”或“不变”)
实验现象 | 实验结论 |
试管内壁有水雾 | 铜绿加热后产生(1) (物质符号) |
固体从绿色变为(2) | 铜绿加热后生成氧化铜 |
气球胀大 |

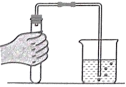
【发现问题】气球为什么会胀大?
【提出猜想】
猜想I:试管内的空气受热膨胀使气球胀大;
猜想Ⅱ:铜绿加热产生氦气使气球胀大;
猜想Ⅲ:铜绿加热产生二氧化碳使气球胀大;
猜想IV:铜绿加热产生一氧化碳气体使气球胀大。
【实验分析】①根据质量守恒定律,可立即判断猜想不成立:
②熄灭酒精灯后,气球稍微缩小但没有缩小到加热前的大小,证明猜想不成立.
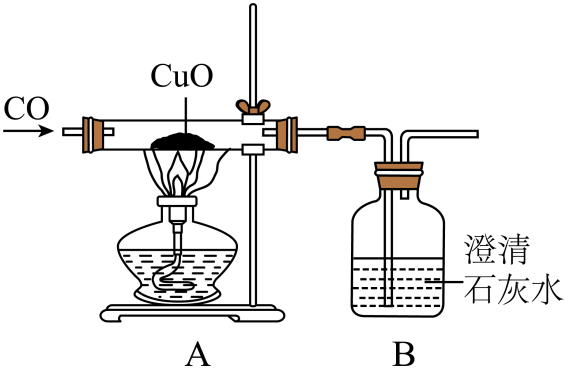
③乙同学用下图装置进行实验,观察到,说明铜绿加热后有CO2产生,产生该现象的化学方程式是,同时还观察到
说明猜想IV不成立。

【实验反思】加热铜绿反应的化学方程式是
回答下面实验问题:

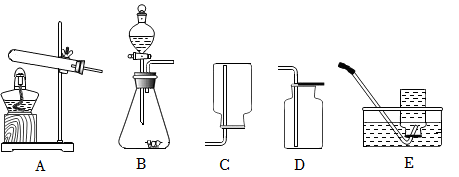
a.用锌粒与稀硫酸反应制氢气
b.用石灰石与稀盐酸反应制二氧化碳
c.用过氧化氢和二氧化锰制氧气
d.加热无水醋酸钠和碱石灰固体混合物制甲烷
实验室用大理石与稀盐酸制取二氧化碳的化学方程式为 。
甲同学试管中加入少量澄清石灰水,观察到试管内 ,由此得到结论:该饮料中含有二氧化碳。
乙同学在试管中加入少量紫色石蕊溶液,观察到试管内 ,乙同学认为也能得到甲同学的结论。
丙同学认为甲同学的方案比较合理,其试管中发生反应的化学方程式为 。
①查阅资料:柠檬酸为无色晶体,易溶于水和酒精;常温稳定,熔点 153℃,熔化后沸腾前分解,分解温度约为 175℃; 柠檬、柑橘等水果中含有柠檬酸。
②乙同学在自己实验的基础上,未增加任何试剂,接着进行了一步实验操作,该操作是 ,可观察到 ,可以确认不是因为柠檬酸而引起紫色石蕊溶液的变色。
选项 | 实验目的 | 实验方案 |
A | 鉴别氮气和二氧化碳 | 分别伸入燃着的木条 |
B | 鉴别木炭粉和铁粉 | 观察颜色 |
C | 除去铜粉中的氧化铜 | 在空气中灼烧 |
D | 除去MgSO4溶液中的少量CuSO4 | 加入足量的镁粉,过滤 |
 检查装置气密性
B .
检查装置气密性
B .  加入石灰石
C .
加入石灰石
C .  加入稀盐酸
D .
加入稀盐酸
D .  检验是否集满
检验是否集满
【查阅资料】
Ⅰ.氧化铜被还原的过程中可能会生成氧化亚铜(Cu2O),Cu2O也能被还原成铜;
Ⅱ.Cu和Cu2O均为不溶于水的红色固体
Ⅲ.Cu与稀硫酸不反应。
Ⅳ.Cu2O能和稀硫酸反应,反应后溶液为蓝色,反应的化学方程式为
【提出问题】反应后生成的红色固体成分是什么?
【作出猜想】
猜想一:红色固体只有Cu;
猜想二:红色固体只有Cu2O
猜想三:红色固体含有。
设计如下实验方案:
实验操作 | 现象 | 结论 |
取少量红色固体于试管中,加入过量的稀硫酸 | 。 | 红色固体含有Cu2O |
甲同学认为猜想二正确,同学们分析后认为他的结论不准确,理由是。
①小组同学通过老师的指导进行了后续实验,证明了猜想三成立。
②该实验在进行操作时,一定要先通入一氧化碳一段时间后再点燃酒精灯,理由是。
为确定CO和CuO反应的最佳温度,小组同学利用原位X射线衍射仪来测定不同温度下反应后的固体物质成分,实验结果如图所示,据图回答下列问题。
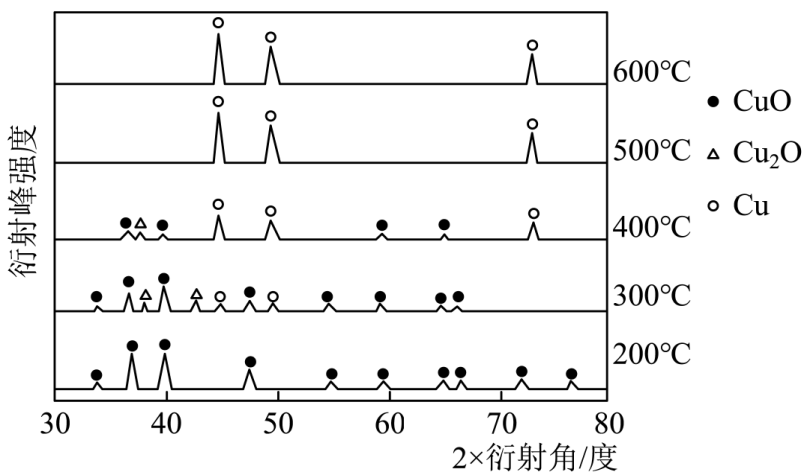
①用CO还原CuO制取纯净的Cu,反应温度至少要控制在℃以上。
②300℃时,反应后的固体中含有:。