
电线是金属的一个应用实例,它利用了金属的什么性质?(答一点即可)
铁的化学性质:

A实验中,反应的化学方程式为,属于反应(填基本反应类型)。
铁的冶炼:
下图是实验室模拟炼铁的装置,请回答以下问题。




药品 | 反应原理 | 制取装置 | 检验该气体方法 |
高锰酸钾 | |||
大理石和稀盐酸 |
 收集氢气
C .
收集氢气
C . 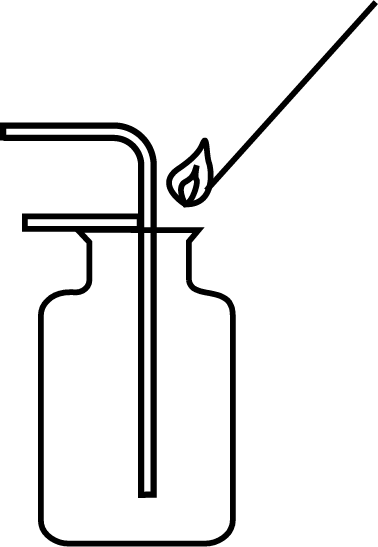 验满二氧化碳
D .
验满二氧化碳
D .  干燥氧气
干燥氧气
实验一:探究分子运动 | 实验二:探究气体制取装置 | 实验三:探究金属活动性 | 实验四:探究热效应的装置 |
|
|
|
|
①实验一:观察到的现象是。
②实验二:该装置可控制反应的发生和停止,通过(填一操作)即可停止反应。
③实验三:金属表面的颜色变化能证明金属活动性 , 有颜色变化的金属丝是,反应一会儿后取出两根金属丝,溶液中一定含有的溶质是(填化学式)。
④实验四:如果观察到U形管中a的液面低于b的液面,则在小试管中加入的固体物质是(填化学式),同时集气瓶中石灰水变浑浊,原因是。
①计算:市售溶液溶质质量分数通常为30%。配制
的
溶液,需要30%的
溶液质量为g。
②量取和混匀:量取所需溶液和水于烧杯中,用玻璃棒批拌,充分混合。
③装瓶贴标签:把配制好的稀溶液装入试剂瓶中,贴上标签,在如图标签中填上相应的内容。
![]()
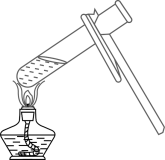 加热液体
B .
加热液体
B . 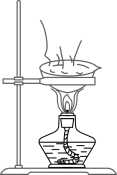 蒸发溶液
C .
蒸发溶液
C .  CO2验满
D .
CO2验满
D . 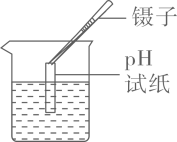 测溶液pH
测溶液pH

【实验探究】
同学们取少量实验后试管b中的溶液,滴入酚酞溶液,溶液,证明稀盐酸和Ca(OH)2溶液发生了反应,反应的化学方程式为。
为进一步探究反应后试管b中酸是否过量,可向试管b中加入____(填序号)。
同学们联想到NaOH溶液与CO2反应也没有明显现象,于是设计图2实验。
(已知通常情况下1体积水最多溶解1体积CO2)
①、若观察到澄清石灰水,则能证明二者发生了反应。
②、如下属于NaOH、Ca (OH)2共同点是(填序号)。
A.易溶于水 B.溶于水明显放热
C.能与SO2反应 D.温度升高,溶解度增大
实验 |
|
|
|
|
异常情况 | 未看到火星四射 | 实际质量偏大 | 澄清石灰水未变浑浊 | 测定结果偏大 |
解释 | A.可能是刚点燃火柴立即伸入 | B.砝码可能生锈 | C.可能是二氧化碳中混有 | D.可能是红磷过量 |