①溶液的作用是。
②的纯度为。

Ⅰ.用的NaOH溶液分别滴定
的盐酸和醋酸溶液各
。滴定过程中溶液pH随
溶液体积变化的两条滴定曲线如图所示:

①取水样于锥形瓶中,加入
溶液(足量),滴入2~3滴淀粉溶液。
②将自己配制的标准溶液(显碱性)装入滴定管中,调整液面,记下读数。
③将锥形瓶置于滴定管下进行滴定,发生的反应为:
试回答下列问题:
①滴定前装有标准液的滴定管排气泡时,应选择下图中的(填标号,下同)。
A. B.
B. C.
C. D.
D.
②若用滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积。
A. B.
C.
D.

已知:常温下,酚酞的变色范围是pH 8.2~10.0,甲基橙的变色范围是pH 3.1~4.4。
Ⅰ.某同学设计如图所示实验,探究反应中的能量变化。

在规格为的滴定管中,若
溶液的起始读数是
, 则此时滴定管中
溶液的实际体积为____(填字母)。

①在清水洗涤后,用标准溶液润洗滴定管次
②取标准液注入滴定管至刻度线0处,并固定在铁架台上
③排气泡后,记下读数
④移取待测水样注入洁净的锥形瓶中,并加入
滴
试液
⑤把锥形瓶放在滴定管的下面,垫上白纸
⑥时,停止滴定,并记下滴定管液面的刻度
将操作⑥补充完整:。
下列操作或误差判断不正确的是(填字母)。
A.滴定过程中,眼睛始终注视锥形瓶中溶液颜色的变化
B.锥形瓶清洗后需要用待测水样润洗次
C.滴定完成后,俯视滴定管读数,会造成滴定结果偏高
D.若滴定结束发现滴定管中出现气泡,则使结果偏低
已知:①[ , X为
、
、
或
]
②(
、
、
)
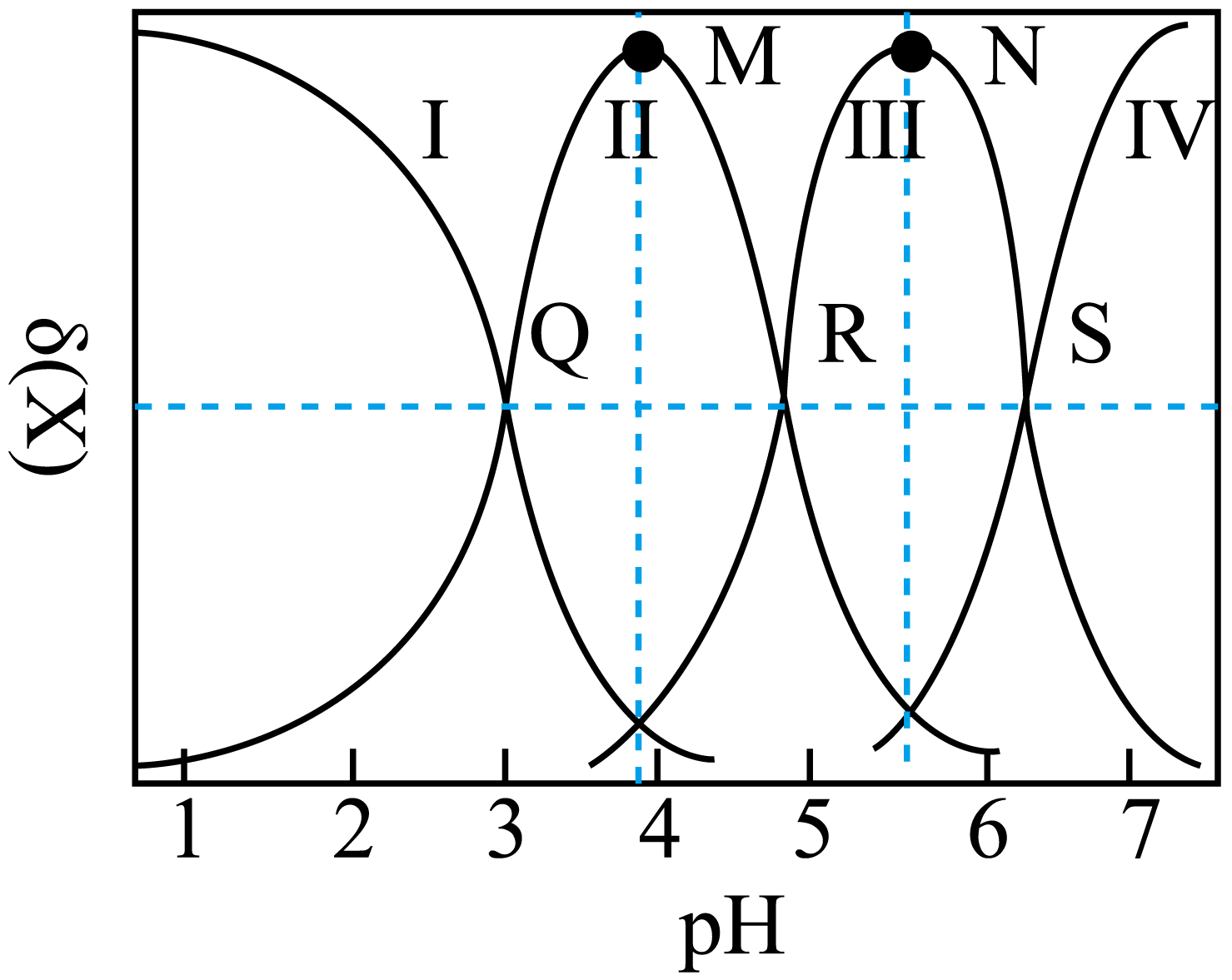
下列叙述错误的是( )
级别 | 特级醋 | 一级醋 | 二级醋 |
醋酸含量(g/100mL) | >6.0 | >4.5 | >3.5 |
实验次数 | NaOH标准溶液 | |
滴定前读数/mL | 滴定终点读数/mL | |
1 | 1.50 | 20.95 |
2 | 2.10 | 21.60 |
3 | 1.20 | 20.75 |
通过计算,该食醋样品中醋酸的含量为(保留两位有效数字)g/100mL,该食醋的级别为。