①该“84消毒液”中NaClO的物质的量浓度为。(保留至小数点后一位)
②现实验室需要的NaClO溶液,某同学用NaClO固体配制该物质的量浓度的溶液。应用托盘天平称取NaClO固体g。配制NaClO溶液时需用的主要仪器有托盘天平、药匙、烧杯、量筒、玻璃棒、、。
③实验时遇到下列情况,会导致溶液物质的量浓度偏高的是(填标号)。
A.容量瓶内壁附有水珠而未干燥处理
B.称量使用的砝码已生锈
C.溶解时使用的烧杯及玻璃棒未洗涤
D.溶解后没有冷却便进行定容
E.定容时俯视刻度线
F.摇匀后发现液面低于刻度线后未做处理
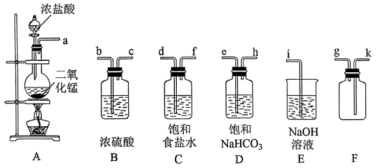
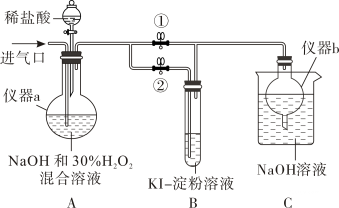
(Ⅰ)制备亚氯酸钠
关闭止水夹②,打开止水夹①,从进气口通入足量 , 充分反应。
装置A中生成的离子方程式为。
停止通气体,再通入空气一段时间后,关闭止水夹①,打开止水夹②,向A中滴入稀硫酸。
开始时A中反应缓慢,稍后产生气体的速率急剧加快,请解释可能的原因。
再次打开止水夹①,。


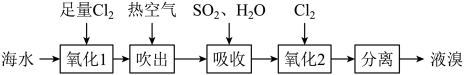
①从海水中提取溴的主要步骤是向浓缩的海水中通入氯气,将溴离子氧化,该反应的离子方程式是。
②可用热空气吹出溴是因为溴的(选填编号)
A.熔点较低 B.熔点较高 C.沸点较低 D.沸点较高

①灼烧海带至灰烬时所用的主要仪器名称是。
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式。反应结束后,再加入作萃取剂,振荡、静置,该步操作用到的仪器名称为,可以观察到
层呈色。