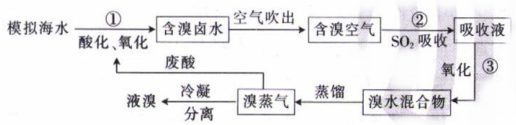

已知:①的浓度较大时易分解爆炸,一般用
或空气稀释到10%以下;实验室也常用稳定剂吸收
, 生成
, 使用时加酸只释放出
一种气体。
②与KI反应的离子方程式为
。
③有关物质的沸点如下表:
物质 | |||
沸点 | 64.7℃ | 100.8℃ | 11℃ |
请回答下列问题:

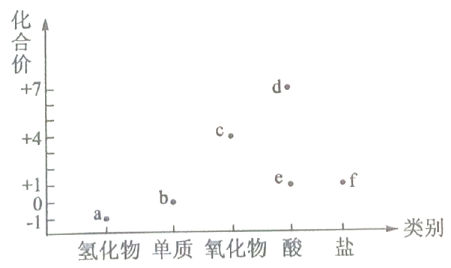
a.只有还原性 b.还原性和酸性 c.只有氧化性 d.氧化性和酸性
HCl | |||
水 | 极易溶 | 可溶 | 极易溶 |
难溶 | 易溶 | 难溶 |
E装置中的试剂是(填化学式)。

图2
泡腾片在使用时需要加水,请补全泡腾片在水中发生反应的离子方程式:
□
。
氯化铁:熔点为306℃,沸点为315℃;易吸收空气中的水分而潮解。工业上采用向500~600℃的铁粉中通入氯气来生产无水氯化铁。
氯化亚铁:熔点为670℃,可升华。工业上采用向炽热铁粉中通入氯化氢来生产无水氯化亚铁。
某化学活动小组用如图所示的装置(夹持装置略去)模拟工业生产制备无水氯化铁。请回答下列问题:

①对比氯化铁中铁元素的质量分数为34.46%,说明含有杂质。
②若要得到较纯净的无水氯化铁,实验装置可进行的改进措施是。