①称取 ,配成
溶液,转移至恒压滴液漏斗中。
②向三颈烧瓶中加入 溶液。
③持续磁力搅拌,将 溶液以
的速度全部滴入三颈烧瓶中,100℃下回流3h。
④冷却后过滤,依次用热水和乙醇洗涤所得黑色沉淀,在 干燥。
⑤管式炉内焙烧2h,得产品3.24g。
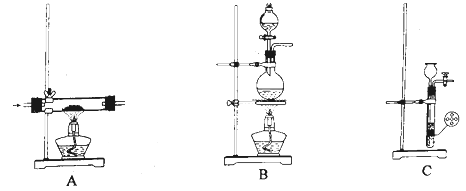
部分装置如图:

回答下列问题:
可供选择的试剂: 、
、
、
、饱和
、饱和
可供选择的发生装置(净化装置略去):

①氮气与氧气在放电的条件下可直接生成NO2
②铵盐都不稳定,受热分解都能生成氨气
③向Fe(NO3)2溶液中滴加稀盐酸,溶液颜色发生明显的变化
④实验室加热氯化铵固体,用碱石灰除去氯化氢的方法制备氨气

①其中叠氮化钠是气体发生剂,受撞击时产生氮气和金属钠。若该反应生成67.2L(标准状况下)氮气时,转移电子的物质的量为。
②高氯酸钾是助氧化剂,在反应过程中与金属钠作用生成氯化钾和氧化钠。鉴别高氯酸钾中钾元素的实验操作及现象为。

|
实验步骤 |
实验现象 |
|
①打开弹簧夹,缓慢通入N2 |
|
|
②加入0.01 mol·L-1的酸性KNO3溶液100 mL |
铁粉部分溶解,溶液呈浅绿色;铁粉不再溶解后,剩余铁粉表面附着少量白色物质 |
|
③反应停止后,拔掉橡胶塞,将圆底烧瓶取下 |
烧瓶内气体的颜色没有发生变化 |
|
④将剩余固体过滤 |
表面的白色物质变为红褐色 |
|
实验步骤 |
实验现象 |
|
①取部分滤液于试管中,向其中加入KSCN溶液 |
溶液无变化 |
|
②将上述溶液分为两份,一份中滴入氯水,另一份中滴加稀硫酸 |
两份溶液均变为红色 |
|
③另取部分滤液于试管中,向其中加入浓NaOH溶液并加热,在试管口放置湿润的红色石蕊试纸 |
有气体生成,该气体使湿润的红色石蕊试纸变蓝 |
(ⅰ)根据以上实验现象,可以判断滤液中存在 (填离子符号)。
(ⅱ)步骤②中滴加稀硫酸后溶液会由浅绿色变成红色,请用离子方程式解释其原因:(写第一步反应)。
(ⅲ)步骤③中生成气体的离子方程式为。