

【猜想假设】(1)NaOH、NaCl;(2)NaOH
【实验探究】取电解后的溶液,进行如下实验:

【收集证据】实验1的反应现象为,实验2发生反应的化学方程式为。

【总结规律】通过探究还可以认识到:上述实验1和实验2的反应都是两种化合物在溶液中以离子的形式,通过一种相互交换成分生成另外两种化合物的方式而发生的复分解反应。


已知:TeO2微溶于水,能与NaOH发生反应,回答下列问题:
 B . 二氧化碳验满
B . 二氧化碳验满  C . 浓硫酸稀释
C . 浓硫酸稀释 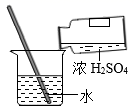 D . 测定溶液pH
D . 测定溶液pH 

反应①:;
反应④:;
试管 编号 | 1 | 2 | 3 | 4 |
加入 试剂 | 无色酚 酞溶液 | 稀盐酸 | 澄清石灰水 | 氯化钡溶液 |
实验 现象 | 有气泡产生 | 有白色沉 淀产生 | 有白色沉 淀产生 |
化学兴趣小组的同学对反应后溶液中溶质的成分进一步探究:小组同学将试管3中的物质过滤,得到滤液A。
【猜想假设】
猜想一:NaOH;
猜想二:NaOH和Na2CO3;
猜想三:;
猜想四:NaOH、Na2CO3和Ca(OH)2。
小组讨论:有同学认为猜想四不成立,原因是。
实验操作 | 实验现象 | 实验结论 |
方案甲:取少量滤液A于试 管中,加入过量的稀盐酸 | 有气泡生成 | 猜想成立 |
方案乙:取少量滤液A于试管 中,加入适量的Ba(NO3)2溶液 | 产生白色 |
碳酸钠溶液呈性,可以和盐酸、氢氧化钙、氯化钡等物质发生反应。