 量筒读数
B .
量筒读数
B .  倾倒液体
C .
倾倒液体
C .  熄灭酒精灯
D .
熄灭酒精灯
D .  过滤
过滤
 B .
B .  C .
C .  D .
D . 
选项 | 实验目的 | 实验方案 |
A | 鉴别羊毛和涤纶 | 灼烧,闻气味 |
B | 除去CaCl2溶液中的少量盐酸 | 加入适量铁粉 |
C | 除去 CO2中混有的少量CO | 点燃 |
D | 鉴别氢氧化钠溶液与澄清石灰水 | 分别取样于试管中,再滴加紫色石蕊溶液 |

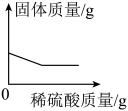 B .
B . 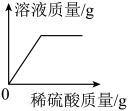 C .
C . 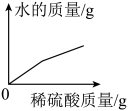 D .
D . 

【查阅资料】草木灰是作物秸秆、枯枝等燃烧后的剩余灰烬,其中富含可溶性钾盐。

【猜想与假设】草木灰中可能含有碳酸钾、硫酸钾中的一种或两种。
【实验探究】
兴趣小组同学另取草木灰水根据表格方案进行实验:
项目 | 实验步骤 | 实验现象及分析 | 实验结论 |
方案 | ①取少量草木灰水于试管中,滴加足量(填试剂名称) | 有大量气泡产生,发生反应的化学方程式为。 | 草木灰中含有碳酸钾 |
②另取少量草木灰水于试管中,滴加足量氯化钡溶液 | 产生白色沉淀 | 草木灰中含有硫酸钾 |
有同学认为步骤②的实验结论不一定正确,理由是,因此需要改进实验。
兴趣小组同学向步骤②中得到的白色沉淀中滴加足量的稀硝酸,观察到的现象是,证明草木灰中含有硫酸钾和碳酸钾。
任务三 验证草木灰古法制碱
古人用草木灰制碱:将草木灰与氢氧化钙悬浊液混合生成氢氧化钾。兴趣小组的同学对此进行实验探究。
资料:常温下Ca(OH)2饱和溶液的pH为12.7,实验配制的K2CO3溶液pH为11.3。
【验证实验】同学们模拟古人制碱的原理,向盛有K2CO3溶液的烧杯中,分3次加入氢氧化钙悬浊液,充分反应后,静置,分别测其溶液的pH(见图)。

小组同学通过分析以上实验数据认为可以证明步草木灰与氢氧化钙悬浊混合后生成了氢氧化钾,依据是。
任务一了解“侯氏制碱法”的产物——和
任务二探究的性质——
溶液呈酸性
【提出问题】溶液呈酸性的原因是什么?
【查阅资料】①溶液呈酸性,是因为溶液中存在较多的。
②在水中全部解离出
和
。
③溶液呈中性,
对溶液的酸碱性没有影响。
【提出猜想】
猜想一:水分子单独起作用,产生较多的 , 使溶液呈酸性;
猜想二:与水作用,产生较多的
, 使溶液呈酸性;
猜想三:。
实验操作 | 实验现象 | 结论 |
向试管中加入一定量的蒸馏水,滴入2滴紫色石蕊溶液 | 溶液呈紫色 | 猜想一不成立 |
向试管中加入一定量的 | 溶液呈紫色 | 猜想二不成立 |
向试管中加入一定量的 | 猜想三成立 |
【拓展与延伸】同学们在查阅资料的过程中还发现:强碱与强酸反应生成的盐溶液呈中性,强酸与弱碱反应生成的盐溶液呈酸性,强碱与弱酸反应生成的盐溶液呈碱性。
已知:①硫酸、盐酸、硝酸属于强酸;②氢氧化钠、氢氧化钾属于强碱;③醋酸属于弱酸;④氨水属于弱碱。
溶液可以看成是强酸与弱碱反应生成的盐溶液。由此可推出醋酸钠溶液呈性,硝酸钾溶液呈性。
属于化肥中的(选填“氮”、“磷”或“钾”)肥。