
计算:需要氯化钠质量克,需要水mL.
实验反思:
若将20g 10%的氯化钠溶液稀释成5%的溶液,需加水mL.
选项 | 实验目的 | 方案 |
A | 鉴别硝酸钠溶液和硫酸钾溶液 | 取样,滴加Ba(NO3)2溶液,观察现象 |
B | 除去粗盐中的难溶性杂质 | 将粗盐研碎、溶解、过滤、蒸发 |
C | 除去CaO中的CaCO3 | 高温加热到固体质量不变 |
D | 探究Mg、Ag、Cu金属的 活动性顺序 | 将两根光亮的镁条分别伸入 硫酸铜溶液和硝酸银溶液中 |
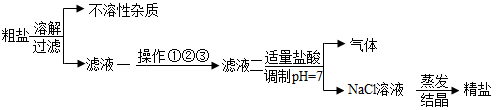
【选择试剂】同学们经过讨论,选择的试剂有:①氢氧化钠溶液②碳酸钠溶液③氯化钡溶液。
【探究过程】取步骤Ⅰ后的粗盐溶液进行下列实验

滴加甲、乙、丙三种试剂的正确顺序最多有种,下列顺序合理的是(填字母)。
A.①②③ B.③②① C.①③②
靖博同学认为,上述实验可以将甲、 乙、丙三种溶液改成两种溶液,分别为(按加入的先后顺序填写溶质的化学式)。