①写出水解反应的离子方程式:,往其溶液中加入下列物质,能促进
水解的是 (填字母)。
A. B.
C.
D.
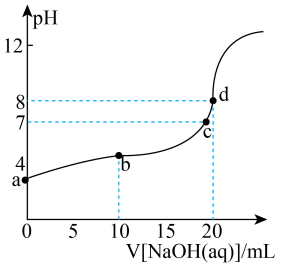
②常温下,向溶液中滴入
的
溶液,溶液的
变化曲线如图所示,d点溶液中
(保留两位有效数字);b点溶液中:
(填“>”“<”或“=”)
。
①常温下要使降低为
, 溶液的
应调至。
②向硫酸铜溶液中通入
气体,该反应的离子方程式为,当溶液中的
时,
。

①若稀释a点溶液,则与稀释前相比,稀释后的溶液中水的电离程度会(填“增大”“不变”或“减小”)。
②若c点溶液中溶质的总物质的量为 , 向c点溶液中加入
的
, 此时溶液满足的元素质量守恒式为。
弱酸 | CH3COOH | HCN | H2CO3 |
电离常数(25℃) | Ka = 1.8×10-5 | Ka=4.3×10-10 | Ka1=5.0×10-7 Ka2=5.6×10-11 |
①常温下,pH相同的三种溶液:A.CH3COONa B.NaCN C.Na2CO3 , 其物质的量浓度由大到小的顺序是(填编号)。
②将少量CO2通入NaCN溶液,反应的离子方程式是。
③室温下,-定浓度的CH3COONa溶液pH=9,用离子方程式表示溶液呈碱性的原因是,溶液中c(CH3COO-)/c(CH3COOH) =

① d点所示的溶液中离子浓度由大到小的顺序依次为。
② b点所示的溶液中c(NH3·H2O)-c(NH4+)=(用溶液中的其它离子浓度表示)。
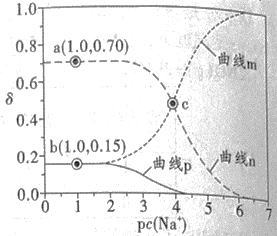
下列说法错误的是( )
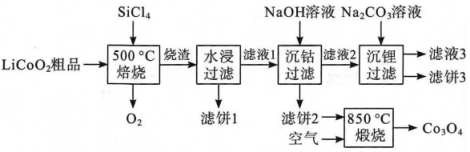
已知:常温下,的电离常数
,
的电离常数
、
,
,
。
回答下列问题:
a.NaOH溶液 b.溶液 c.氨水
①(填“>”“<”或“=”)1。
②三种溶液中由水电离出的的浓度的关系是(用a、b、c表示)。