
①加热反应前通的目的是。
②A中仪器X的名称是,其作用是。
③E中收集的物质含有(写化学式)。
④尾气经处理后可循环使用。
①中存在的化学键有(填序号)。
a.配位键 b.氢键 c.离子键 d.金属键
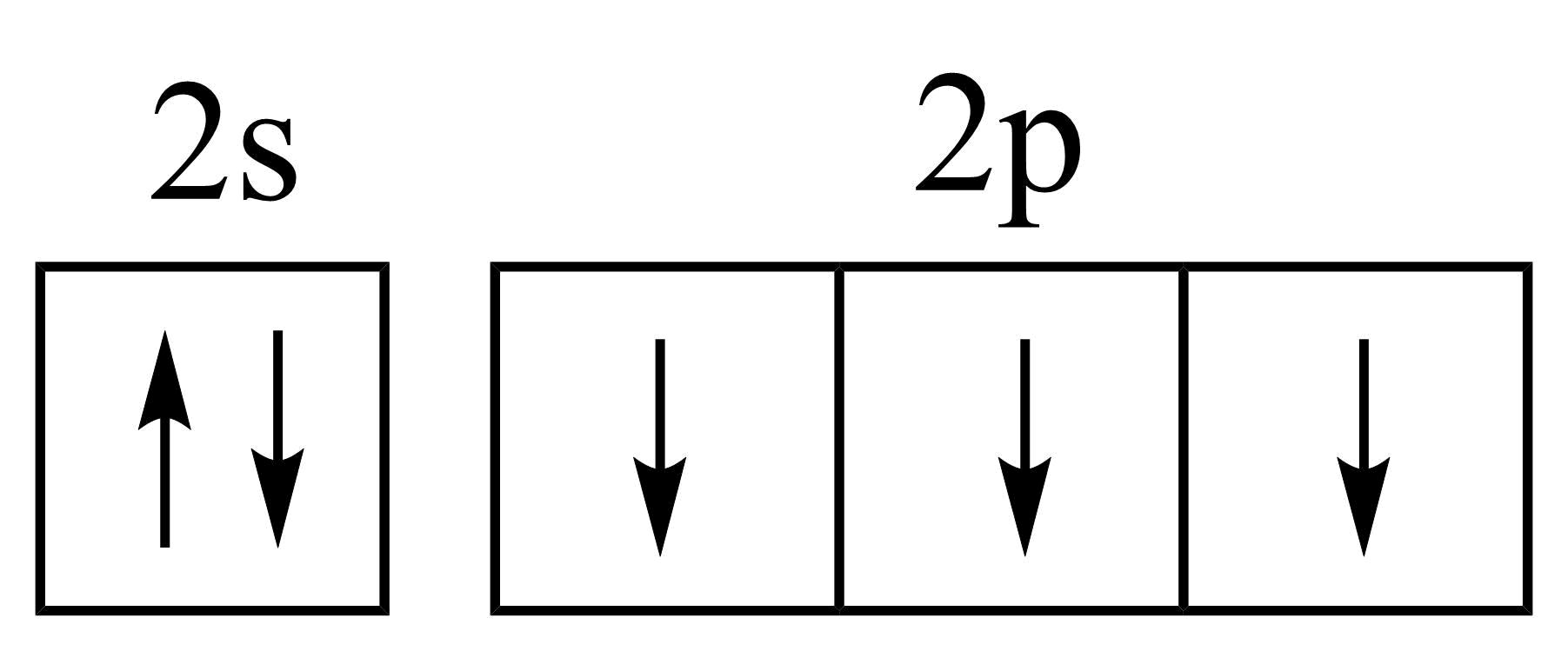
②该暗绿色晶体的化学式为。
 C .
C . 
已知:①;
②焦亚硫酸钠()常用作食品抗氧化剂;
③氧化性:。
回答下列问题:
a.CoO
b.
c.KOH


选项 | 实验操作及现象 | 结论 |
A | 向重铬酸钾溶液中加水,溶液颜色变浅 | 增加水的用量,平衡 |
B | 向含酚酞的 |
|
C | 向硫酸铜溶液中滴加浓氨水至过量,溶液先产生蓝色沉淀,然后沉淀溶解变为深蓝色溶液 |
|
D |
|
|
 B . 基态
B . 基态 C .
C .  D . 铵根离子的电子式:
D . 铵根离子的电子式:

①周围距离最近且等距的
数目为.
②设晶胞边长为为阿伏加德罗常数的值,该晶体的密度为
.

晶体中
与
的作用力类型是,
的空间构型为.

已知:①“碱浸”时,铜、锑转化为难溶氢氧化物或氧化物,碱浸液含有Na2TeO3、Na3AsO4。
②“酸浸”时,锑元素反应生成难溶的Sb2O(SO4)4浸渣。
回答下列问题: