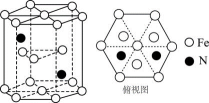



A.离子键 B.配位键 C.π键 D.σ键 E.氢键


 B . 用电子式表示
B . 用电子式表示
图1 图2
图2
①当投料比大于80时,乙醇酸甲酯的选择性降低,其原因是。
②已知投料比为60时,草酸二甲酯的转化率为 , 该条件下不发生反应Ⅲ,则最终收集的流出气中甲醇蒸气的分压为
(计算结果保留二位小数)。
①当反应温度高于时,乙二醇的选择性降低,原因是。
②请在图3(见答题卷)上画出乙醇酸甲酯的产率随温度的变化。
已知:

比较键角 ,
(填“>”、“<”或“=”),理由是。

图2