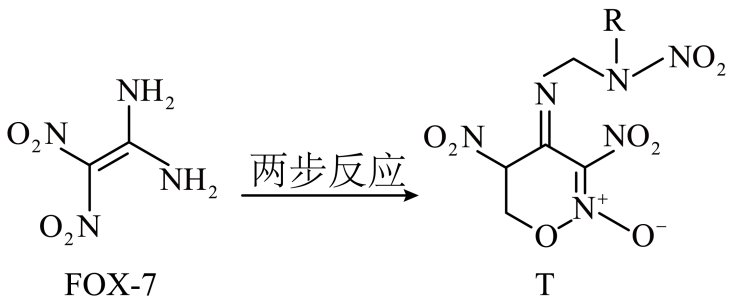
D . HCl的形成过程:
D . HCl的形成过程: 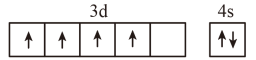 B .
B . 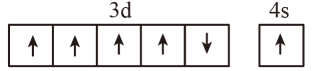 C .
C .  D .
D . 

①中Fe3+的杂化轨道类型为(填字母)。
A. B.
C.
D.
②配体SCN-和H2O的键角大小:SCN- H2O (填“<”“>”或“=”。用杂化轨道理论解释,其原因为。
③SCN-中所有原子均满足最外层8电子结构。写出SCN-的电子式。

①以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的相对位置,称作原子坐标。如1号原子的坐标为 , 2号原子的坐标为
, 则3号Fe原子的坐标为。
②若晶胞参数分别为apm、bpm、cpm,阿伏加德罗常数的值为NA , 则晶体的密度为 g∙cm-3 (列出计算表达式)。