

总反应:CO(g)+N2O(g) CO2(g)+N2(g) ΔH=kJ·mol-1;该总反应的决速步是反应(填“①”或“②”)

①表示N2O的转化率随的变化曲线为曲线(填“I”或“Ⅱ”);
②T1T2(填“>”或“<”);
③已知:该反应的标准平衡常数 , 其中pθ为标准压强(100kPa),p(CO2)、p(N2)、p(N2O)和p(CO)为各组分的平衡分压,则T4时,该反应的标准平衡常数Kθ=(列出计算式)。

①盐酸的浓度 ②镁条的表面积 ③溶液的温度 ④Cl-的浓度
①
②
,
。
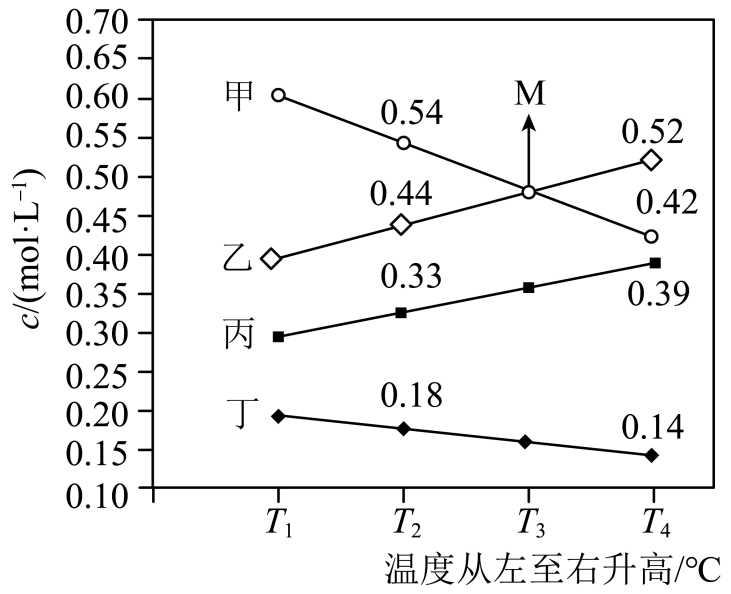
①甲是(填化学式),写出该反应的化学方程式:。
②正反应(填“>”“<”或“=”)0,判断依据是
③T3℃时NH3的平衡转化率为。
