甲 | 乙 | 丙 | 丁 |
|
|
|
|
选项 | 劳动项目 | 解释 |
A | 用SO2漂白纸浆 | SO2具有还原性 |
B | 用铝制容器贮运浓硝酸 | 铝遇浓硝酸钝化 |
C | 模具注入熔融钢水之前必须干燥 | 铁与H2O在高温下会反应 |
D | 用固体管道疏通剂(主要成分为NaOH和铝粉)疏通管道 | 与铝粉和NaOH溶液反应产生气体有关 |

已知:①“碱浸”时,铜、锑转化为难溶氢氧化物或氧化物,碱浸液含有Na2TeO3、Na3AsO4。
②“酸浸”时,锑元素反应生成难溶的Sb2O(SO4)4浸渣。
回答下列问题:
下列有关说法不正确的是____。


①x=。
②若石墨层内的大π键可表示为(上标表示电子总数,下标表示轨道数),则平均每个KCx单元中的大π键可表示为(用具体的数据表示)。
③KCx中,石墨层间,每个钾离子相距最近且等距的钾离子有个。
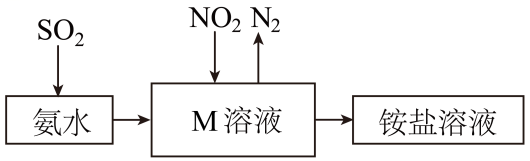
在一定条件下NH3可将NO2还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。
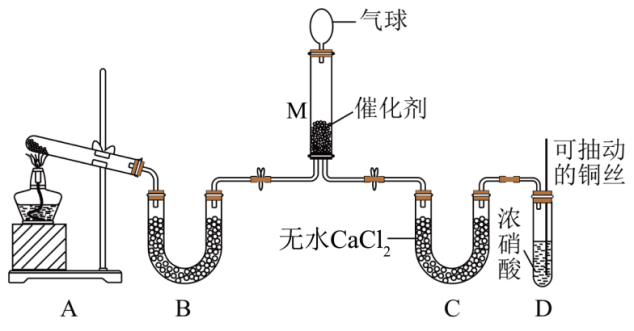
装置D中发生反应的离子方程式是。