
钠元素在自然界中分布很广,储量极为丰富,常在氯化钠、碳酸钠、硫酸钠等物质中存在。19世纪初,英国化学家戴维在实验室中首次制得了金属钠。钠是一种银白色金属,质软,密度为0.97g/cm3 , 熔点为97.8℃,金属钠的性质很活泼,能与许多物质发生化学反应。钠暴露在空气中,与氧气反应生成氧化钠(Na2O),钠在空气中燃烧,生成淡黄色的过氧化钠(Na2O2)。钠和钾形成的合金熔点低,常温下呈液态,可用作中子反应堆的热交换剂。利用钠的强还原性,在一定条件下可以将钛(Ti)、锆(Zr)等金属从其氯化物中置换出来,例如,钠可以在高温条件下与四氯化锆反应生成氯化钠和锆。
【提出问题】“锡纸”中的金属是铝还是锡?
【查阅资料】锡(Sn)与酸或金属的化合物溶液反应生成+2价的锡的化合物。
【做出假设】猜想Ⅰ:“锡纸”中的金属是锡;
猜想Ⅱ:“锡纸”中的金属是铝。
实验过程中使用的金属均已打磨过,其目的是。
实验序号 | 实验操作 | 实验现象 | 实验分析与结论 |
实验一 |
| 猜想(填“Ⅰ”或“Ⅱ”)成立。装置③中反应的化学方程式为。 | |
实验二 |
| ③中有固体析出 |
下列物质的溶液可以替代实验二中的氯化锌溶液完成上述实验的是____(填字母)。
选项 | 实验目的 | 实验方法 |
A | 鉴别铁粉和氧化铜粉末 | 观察颜色 |
B | 鉴别NaCl溶液和NaOH溶液 | 取样,滴加CuSO4溶液,观察现象 |
C | 除去CaCl2溶液中混有的盐酸 | 加入过量的CaO,过滤 |
D | 除去CO2气体中混有的HCl气体 | 通过盛有NaOH溶液的洗气瓶 |
 加热两份等质量的氯酸钾制取氧气
B .
加热两份等质量的氯酸钾制取氧气
B . 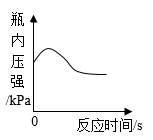 用红磷燃烧法测定空气中氧气含量时瓶内压强的变化
C .
用红磷燃烧法测定空气中氧气含量时瓶内压强的变化
C . 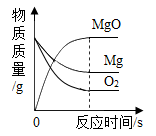 等质量的镁和氧气充分反应
D .
等质量的镁和氧气充分反应
D . 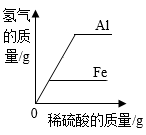 向等质量的铝粉和铁粉中分别加入溶质质量分数相等的稀硫酸
向等质量的铝粉和铁粉中分别加入溶质质量分数相等的稀硫酸