甲 | 乙 | 丙 | |
烧杯+稀硫酸/g | 250 | 200 | 200 |
加入的铁样品/g | 9 | 9 | 14 |
充分反应后,烧杯+剩余物/g | 258.7 | 208.7 | 213.7 |
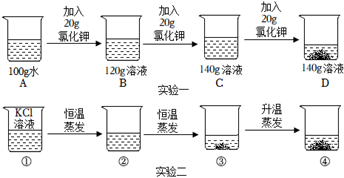
请你认真分析数据,回答下列问题:(烧杯的质量为77.5g;计算结果精确到1%)
实验分组 | 第1组 | 第2组 | ||||||
催化剂 | Co4N/Al2O3 | Co/Al2O3 | ||||||
温度/℃ | 300 | 320 | 340 | 360 | 300 | 320 | 340 | 360 |
CO2转化率(%) | 84.4 | 85.3 | 86.8 | 90.1 | 37.6 | 48.8 | 54.9 | 59.8 |
分析上表数据可知:催化剂(选填“Co4N/Al2O3”或“Co/Al2O3”)的催化性能更好。
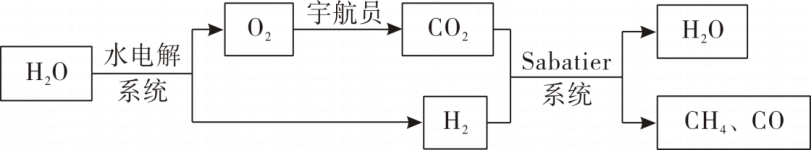
【实验目的】探究溶解过程中,溶液温度的变化情况。
【查阅资料】⑴物质溶解于水的过程包括吸收热量(Q吸)的扩散过程和放出热量(Q放)的水合过程。⑵实验条件下,水的凝固点为0℃、沸点为100℃。
【提出猜想】物质溶解过程中,溶液的温度可能升高或降低成不变。
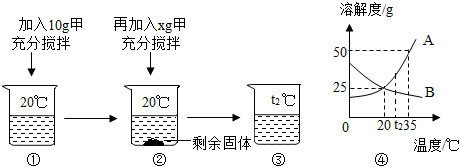
【实验探究】某探究小组的同学设计了如图所示的两种方案,在图2所示方案中,每次加入物质b之前均使用温度计控制热水温度,使之保持在99℃。
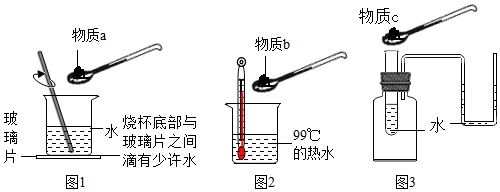
【拓展实验】按照图3所示进行实验,若物质c为氢氧化钠,则U形管内的左边液面将(填“高于”或“低于”或“等于”)右边液面。
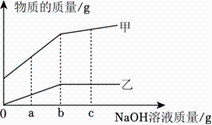
【反思交流】该小组的同学进一步就物质溶解过程中溶液温度变化的原因展开了讨论,分析得出:若Q吸Q放(填“>”或“<”或“=”),则溶液温度下降;若Q吸与Q放的相对大小与之相反,则溶液温度上升。
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | |
| 溶解度/g | 甲 | 0.18 | 0.16 | 0.14 | 0.12 | 0.09 |
| 乙 | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | |
| 丙 | 13.3 | 31.6 | 63.9 | 110 | 169 | |