|
|
|
|
A.配制 | B.闻气体气味 | C.验证碳酸氢钠受热易分解 | D.尾气 |
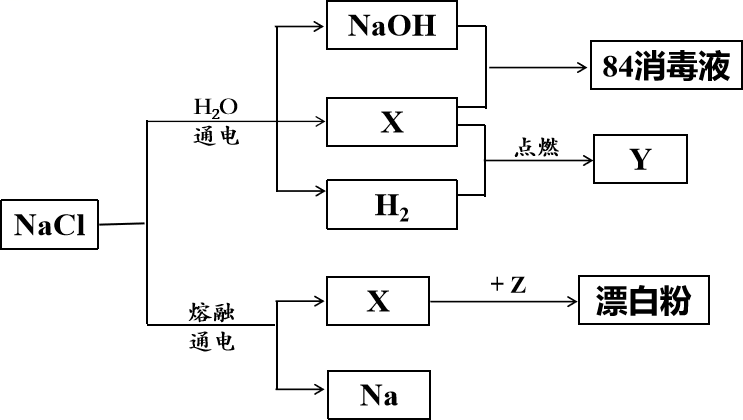
①若试剂Y是 , 转化原理用离子方程式表示为
,
属于(填“氧化产物”或“还原产物”)。
②若试剂Y是Fe,转化原理用离子方程式表示为,化工生产中②比①好,从物质利用率角度考虑,其原因是。
选项 | A | B | C | D |
装置 |
|
|
|
|
实验目的 | 验证Na与水反应放热 | 测定氯水的pH | 比较 | 完成铁粉与水蒸气的实验 |
选项 | 化学事实 | 类推结论 |
A | Al与 | Na比Al活泼,也能从 |
B |
|
|
C | 溶解度: | 溶解度: |
D |
| 金属氧化物都属于碱性氧化物 |
|
|
|
|
A.制备 | B.验证铁与水蒸气反应能生成 | C.转移溶液 | D.比较 |
| 实验操作及现象 | 实验结论 |
A | 某溶液中先加入 沉淀不消失 | 该溶液不一定有 |
B | 向饱和 | 氯水中含 |
C | 向饱和 | 溶解度: |
D | 把绿豆大的 | 金属性: |
①配制溶液过程中用托盘天平称量固体的质量为g。
②定容时,加蒸馏水不慎超过刻度线,处理的方法是。
装置 | 实验 | 试剂a | 现象 |
| 甲 | 4mL | 产生白色沉淀 |
乙 | 4mL | 产生白色沉淀及大量气体 | |
丙 | 4mL | 产生白色沉淀及大量气体 |
为了探究白色沉淀的成分,设计了热分解实验,其装置如图所示:
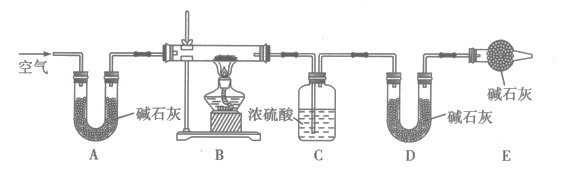
将实验乙、丙所得沉淀分别置于装置B中使样品完全分解,实验结束后,数据记录如下:
样品 | 加热前样品质量/g | 加热后样品质量/g | 装置C增重/g | 装置D增重/g |
实验乙样品 | 10.4 | 6.8 | 3.6 | 0 |
实验丙样品 | 22.4 | 16.2 | 1.8 | 4.4 |
①实验甲产生白色沉淀反应的离子方程式为。
②装置E的作用是。
③通过热分解实验可判断实验乙所得白色沉淀的成分为(填化学式),实验乙反应的离子方程式为。
④实验丙所得白色沉淀的化学式可表示为 , 则
。
①实验室配制溶液的操作是取一定量
固体溶于浓硝酸中,加入蒸馏水稀释至指定体积。其中,浓硝酸的作用是.
②对溶液进行加热,溶液变为红褐色,由此判断,
0(填“>”或“<”),判断理由是.
序号 | 操作 | 现象 |
Ⅰ | 向乙中加入少量铁粉,振荡 | 溶液颜色比甲浅 |
Ⅱ | 向丙中加入少量 | 溶液颜色与甲无明显变化 |
Ⅲ | 向丁中滴加足量的新制氯水,振荡 | 溶液颜色变为黄色 |
①参照组甲溶液颜色为.
②解释产生实验Ⅰ中现象的原因:.
③实验Ⅲ中产生异常现象的原因可能是,为了验证该猜想,请设计简单实验:.