
①t1℃时,将40g硝酸钾加入到100g水中,充分搅拌,形成溶液(填“饱和”或“不饱和”);
②P点表示t1℃时,硝酸钾的溶解度氯化钠的溶解度(填“大于”“等于”或“小于”);
③将t2℃时一定质量的硝酸钾饱和溶液降温到t1℃,所得溶液的溶质质量分数(填“增大”“不变”或“减小”)。

A.量取水时俯视读数 B.配完后将溶液转移至试剂瓶时洒出了一些
C.将量好的水从量筒里倒入烧杯时,量筒内壁有少量的水残留
D.称量时砝码放左盘食盐放右盘
主要成分 | 次氯酸钠 |
含量 | 5% |
剂型 | 液体 |
总量 | 500mL |
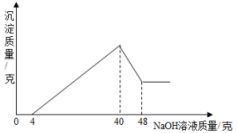
(提示:Al(OH)3+NaOH=NaAlO2+2H2O,NaAlO2易溶于水)

①通过计算,配制上述食盐溶液需要固体氯化钠15g,水85mL
②将托盘天平调节平衡后,把固体氯化钠直接放在左盘上称量,然后倒入烧杯中
③用量筒量取85mL水,倒入盛有氯化钠的烧杯中,用玻璃棒搅拌使其全部溶解
④将配制好的溶液装入试剂瓶中,盖好瓶塞,贴好标签
在上述实验操作步骤中,存在明显操作失误的步骤是(填序号)。
表一 食盐溶液溶质质量分数与密度对照表

|
溶质质量分数 |
溶液密度(g/cm3) |
|
2% |
1.01 |
|
6% |
1.03 |
|
10% |
1.07 |
|
15% |
1.10 |