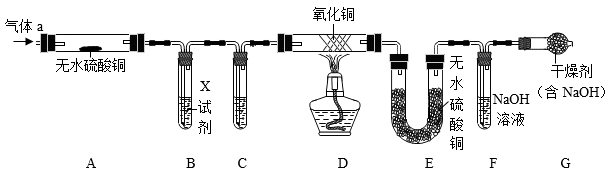
已知:
I.无水硫酸铜粉末遇水由白色变蓝色。
Ⅱ.① ;②
【提出问题】该烧杯内的溶质是什么?
【猜想假设】猜想一:Na2SO4
猜想二:Na2SO4和NaOH
猜想三:Na2SO4和H2SO4
猜想四:Na2SO4、NaOH和H2SO4
【实验探究】
甲、乙、丙三位同学分别设计了如下的实验方案,请你帮助他们完成实验报告的相关内容。
实验方案 | 实验现象 | 实验结论 | |
方案1 | 甲同学取少量烧杯内的溶液于试管中,滴入酚酞试液 | 溶液无明显变化 | 猜想二不成立 |
方案2 | 乙同学取少量烧杯内的溶液于试管中,滴加适量的CuSO4溶液 | ||
方案3 | 丙同学取少量烧杯内的溶液于试管中,加入锌粒,反应的化学方程式为:。 | 有气泡生成 | 猜想成立 |
该同学实验操作是____。(填字母)
装置
的目的是除去
中的水蒸气,试剂
的名称。
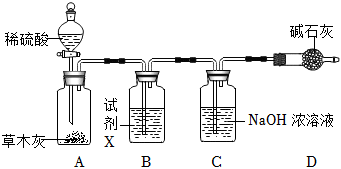
实验时称取
草木灰样品,反应后称得
装置增重
, 则草木灰样品中碳酸钾的质量分数为
用含
和
的代数式表示
。
实验测得的结果略小于实际含量,除了装置漏气的因素外,还可能存在的原因是。
【查阅资料】:①铜锈俗称铜绿,化学式为Cu2(OH) 2CO3 , 受热易分解:
②无水CuSO4为白色粉末,遇水变蓝:
③碱石灰是CaO和NaOH的固体混合物,能吸收二氧化碳和水蒸气;
④碳粉不与稀盐酸反应,也不溶于稀盐酸;
【发现问题】:小组同学将少量铜锈放入试管中加热,发现固体由绿色变成黑色。
探究一:生成的黑色固体成分。
猜想二:黑色固体是CuO;
猜想三:黑色固体是
实验操作 | 实验现象 | 实验结论 |
取少量样品于试管中,加入足量稀硫酸 | 黑色固体溶解(填“全部”或“部分”),溶液变色 | 猜想二正确 |
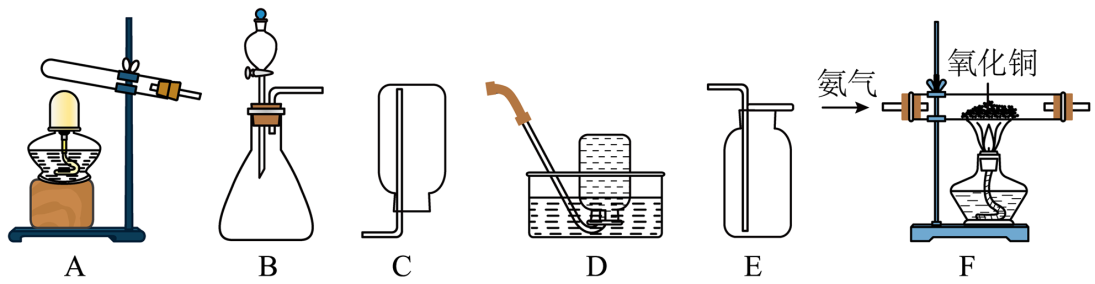
【进行实验】:选择如图所示装置进行验证。

步骤一:连接A 和 B,打开弹簧夹,通入一段时间的空气;
步骤二:关闭弹簧夹,依次连接装置 A→B→ (选填“C→D”或“D→C” );
步骤三:点燃酒精灯,观察到固体由绿色变成色后,停止加热。当观察到无水 CuSO4变蓝色,说明铜锈受热分解生成了,则进一步。当观察到装置 D中澄清石灰水,说明铜锈受热分解生成了 CO2。
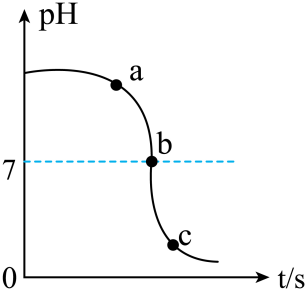
小雪认为该低钠盐溶液呈酸性,她的判断依据是 。
实验步骤 | 实验现象 | 实验结论 |
分别用a、b、c三支试管取样,各加入一定量碳酸钠溶液 | a中有气泡产生 | a中物质是 |
b中无明显现象 | b中物质是食盐水 | |
c中 | c中物质是澄清石灰水 |
写出a试管中发生反应的化学方程式: 。把c试管反应后的物质进行过滤,得到滤液。
猜想一:Na2CO3和NaOH;猜想二:NaOH;猜想三:。
提示:Ca(OH)2微溶于水。
实验步骤 | 实验现象 | 实验结论 |
取一定量滤液于试管中,加入一种盐溶液(写溶质化学式)。 | 有白色沉淀 | 猜想一正确 |
写出上述有白色沉淀生成的化学方程式:。
同学们还对a试管反应后废液的酸碱性感兴趣,决定用pH试纸测定其pH值。
用pH试纸测定a试管反应后废液酸碱性的过程 | 测定结果 |
在白瓷板上放一小片pH试纸,用玻璃棒蘸取。 | pH<7(废液显酸性) |
【提出问题】得到的红色粉末是什么?
查阅资料:Cu2O是红色,易与稀硫酸反应:Cu2O+H2SO4=CuSO4+Cu+H2O
【猜想假设】红色粉末是①Cu;②Cu2O;③。
实验步骤 | 实验现象 | 实验结论 |
取红色粉末于试管中,加入足量稀硫酸 | 红色粉末中含有Cu2O |
【猜想】白色固体为:①MgCO3;②Mg(OH)2;③xMgCO3•yMg(OH)2•zH2O。
【实验1】称取3.64g白色固体,加入过量的稀盐酸,出现气泡,则猜想 (填序号,下同)不成立。将产生的气体全部通入过量的澄清石灰水中,产生3.0g沉淀,则猜想 成立。
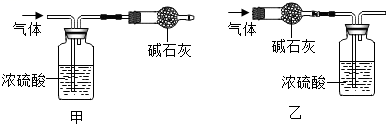
实验测得浓硫酸的质量增加1.44g,碱石灰的质量增加2.64g,则x:y:z=。
Ⅰ.石笋和钟乳石的形成过程
石灰石遇到溶有二氧化碳的水会生成易溶于水的碳酸氢钙[Ca(HCO3)2],请写出该反应的化学方程式:。溶有碳酸氢钙的水遇热或当压强突然变小时,就会分解生成碳酸钙,沉积在洞底的形成石笋,沉积在洞顶的形成钟乳石。
探究活动:探究白色固体的成分
【作出猜想】猜想1:只含 ;猜想2:只含 Ca(HCO3)2;猜想3:含 Ca(HCO3)2、CaCO3
操作步骤 | 现象 | 结论 |
①取少量白色固体研碎后,置于烧杯中,加入足量水充分搅拌 | 猜想2不正确 | |
②取①中少量上层清液于试管中,滴入稀盐酸 | 无明显现象 | 猜想 正确 |
