某化学课堂围绕“酸碱中和反应”开展探究活动。
【查阅资料】Na2SO4溶液、BaCl2溶液均呈中性
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中。
【假设猜想】
请你将猜想1补充完整。
猜想1:
猜想2:有Na2SO4和H2SO4
猜想3:有Na2SO4和NaOH
取反应后的溶液分别加入试管A、B中
实验序号 | 操作 | 现象 | 结论 |
1 | 向A中滴加少量CuSO4溶液 | 无明显现象 | 不含 |
2 | 向B中滴加BaCl2溶液 | 含有H2SO4 |
有同学认为实验2结论不够严谨,理由是(用化学方程式解释)。
实验序号 | 操作 | 现象 | 结论 |
3 | 另取少量反应后的溶液于试管中,加入 | 有气泡产生 | 猜想2成立 |
a.废液处理呈中性才能排放
b.处理废液时应先分析成分再进行处理
c.处理该废液时加入过量的氢氧化钠溶液
 B .
B .  C .
C .  D .
D . 

选项 | 实验目的 | 实验方案 |
A | 除去CO中的CO2 | 将气体通过灼热的CuO |
B | 区分氢氧化钠溶液和纯碱溶液 | 取样,加入无色酚酞溶液 |
C | 验证Cu与Ag的金属活动性 | 取样,分别滴加稀盐酸 |
D | 比较呼出气体与空气中O2的含量 | 分别伸入燃着的小木条 |
①图中仪器①的名称是。

②实验室制取CO2 , 为获得平稳的气流,应选择图中的发生装置(填字母),化学方程式为。
③收集一瓶CO2并进行性质检验。
操作 | 现象 | 结论 |
| 如图观察到的实验现象有 Ⅰ:, Ⅱ:。 | CO2能与水反应 |
该实验中使紫色石蕊试液变红的物质是Ⅲ。 | ||
配方 | 母液A | 母液B | 母液C | |||
药品 | 含量(g/L) | 药品 | 含量(g/L) | 药品 | 含量(g/L) | |
配方一 | NH4NO3 | 140.0 | 15.0 | 18.60 | ||
KNO3 | 165.0 | KH2PO4 | 10.0 | 13.90 | ||
17.7 | ||||||
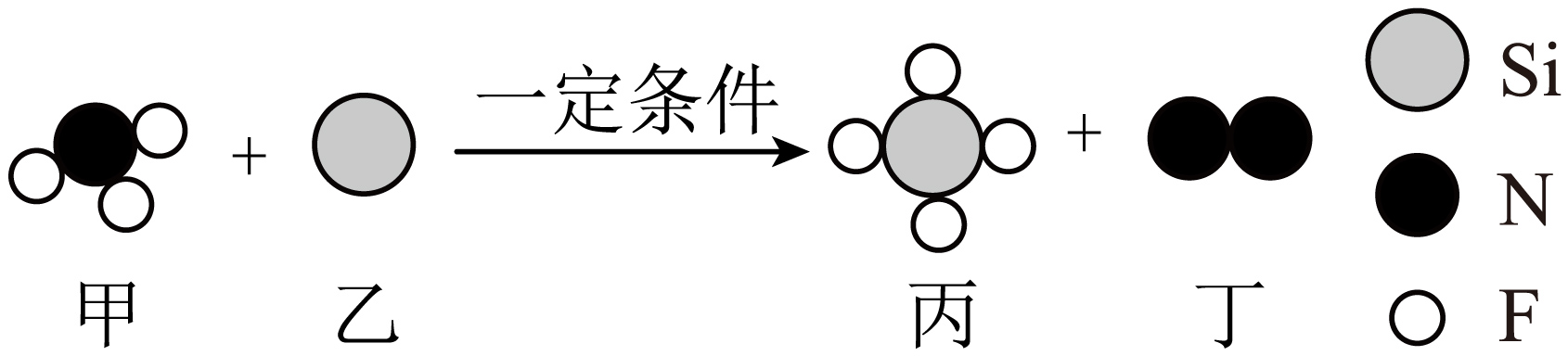
二氧化碳是由(填粒子名称)构成的。
工业上,煅烧石灰石(主要成分是CaCO3)来制取二氧化碳,该反应的化学方程式为。
根据图回答问题。向充满CO2的软矿泉水瓶中倒入澄清石灰水,旋紧瓶塞后充分振荡,能观察到的现象是软矿泉水瓶收缩变瘪和,该反应的化学方程式为。
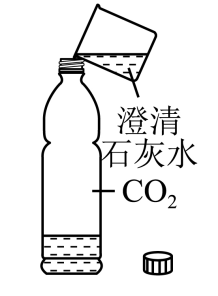
液态二氧化碳灭火的原理是。
【实验探究】将氢氧化钾溶液与稀硫酸混合,观察不到明显现象,为证明氢氧化钾溶液与稀硫酸发生了反应,三位同学进行了以下实验。
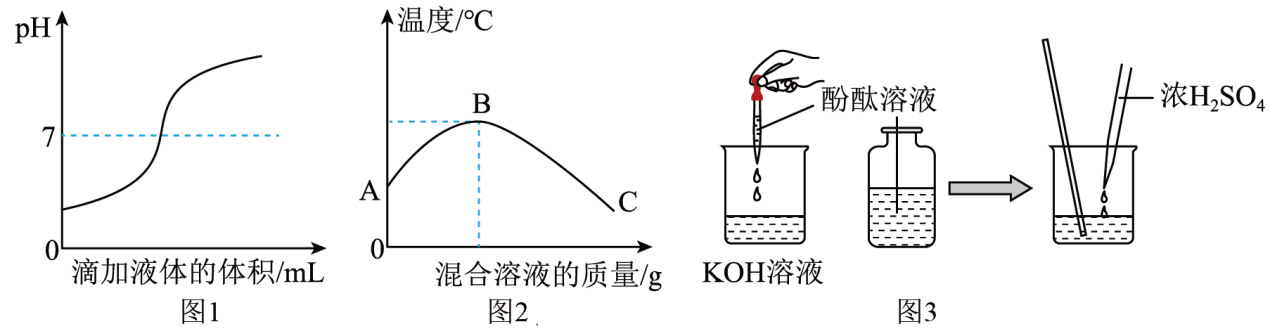
甲同学在实验过程中测得pH变化如图1所示,则该同学是将(填字母序号)。
a.氢氧化钾溶液滴入稀硫酸中
b.稀硫酸滴入氢氧化钾溶液中
乙同学在实验过程中测得反应混合溶液的温度变化如图2所示,说明稀硫酸与氢氧化钾溶液发生的反应是(填“放热”或“吸热”)反应。图2中B点表示的含义是。
丙同学通过图3所示实验,他观察到溶液由红色变成无色,也证明氢氧化钾溶液与稀硫酸发生了化学反应,反应的化学方程式为。
【猜想与假设】
猜想一:只有K2SO4;猜想二:有K2SO4和H2SO4;猜想三:有K2SO4和KOH
【进行实验】
为了验证猜想,学习小组选用Fe2O3粉末、BaCl2溶液,进行如下探究:
实验方案 | 实验操作 | 实验现象 | 实验结论 |
方案一 | 取少量反应后的溶液于试管中,加入Fe2O3粉末 | 、 | 溶液中有H2SO4猜想二正确 |
方案二 | 取少量反应后的溶液于试管中,滴加BaCl2溶液 | 产生白色沉淀 | 溶液中有H2SO4 , 猜想二正确 |
【评价与反思】
丁同学针对上述方案提出疑问,认为方案二是不合理的,理由是。